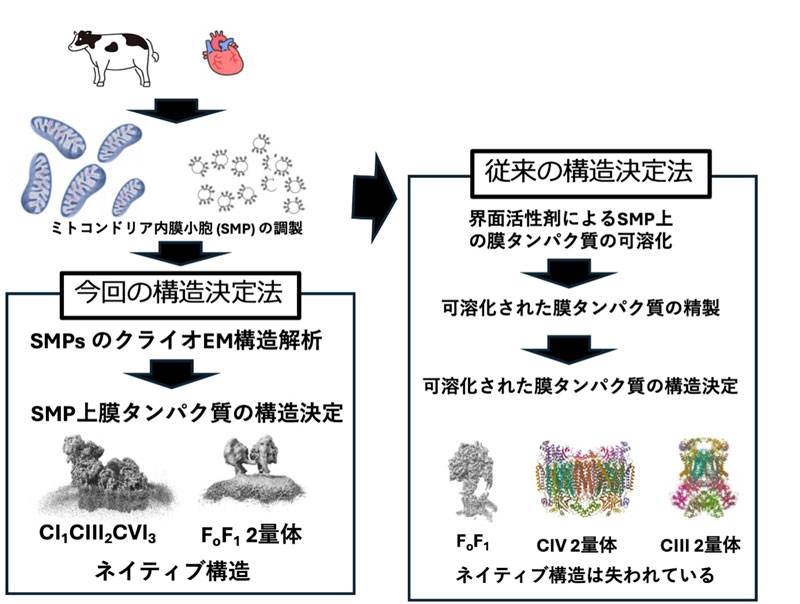
村井正俊 農学研究科教授、横山謙 京都産業大学教授を中心とする共同研究グループは、ウシ心臓由来ミトコンドリアから調製したサブミトコンドリア粒子を用い、クライオ電子顕微鏡による単粒子解析によって、ミトコンドリア内膜タンパク質を、膜を壊さない本来の状態(ネイティブ状態)で構造解析しました。
その結果、ATP合成酵素(FoF1)がIF1タンパク質で連結された二量体として存在し、さらにそれらが会合した四量体構造がミトコンドリア内膜中に実在することを初めて明確に示しました。この四量体は膜を強く湾曲させ、ミトコンドリアのクリステ形成に重要な役割を果たすと考えられます。また、ATP合成酵素の回転リング中心に安定した脂質が存在するという従来の仮説は支持されませんでした。さらに、呼吸鎖超分子複合体について、従来知られていた構成に加え、CI1CIII2CIV₃という新規構成や、CI₂CIII₂CIV₆からなる巨大メガ複合体の存在を同定し、呼吸鎖複合体が多様な組み合わせで膜中に存在することを明らかにしました。
本成果は、ミトコンドリア膜タンパク質を少量試料からネイティブ状態で直接構造解析できる新たな手法の有効性を示すものであり、疾患関連ミトコンドリア研究や患者生検試料を用いた構造解析への応用、さらには膜タンパク質構造研究のパラダイム転換につながることが期待されます。
本研究成果は、2026年3月17日に、国際学術誌「Nature Communications」にオンライン掲載されました。
研究者のコメント
「これまでミトコンドリア膜タンパク質の構造・機能解析には、大量の試料と膨大な労力が必要でした。本研究により少量試料からの構造決定が可能となり、患者生検試料や培養細胞を用いた解析への道が開かれました。ミトコンドリアが関与する生命現象や疾患の分子基盤解明が大きく前進すると期待しています。」(横山謙、村井正俊)
【DOI】
https://doi.org/10.1038/s41467-026-70578-x
【KURENAIアクセスURL】
http://hdl.handle.net/2433/300827
【書誌情報】
Atsuki Nakano, Takahiro Masuya, Shinsuke Akisada, Moe Ishikawa-Fukuda, Kaoru Mitsuoka, Hideto Miyoshi, Masatoshi Murai, Ken Yokoyama (2026). Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane. Nature Communications, 17, 4075.