茶本健司 医学研究科特定教授、Zhang Rongsheng 同博士課程学生らは、キラーT細胞とヘルパーT細胞を同時に活性化する非自己ペプチドが細胞内に存在すると、その配列内容に依存せず広範な腫瘍免疫を誘導できる「キメラ型MHCクラスI・IIエピトープ」を開発しました。この様なペプチドの条件として、1)MHCクラスI・IIエピトープが単一のペプチドに存在すること、2)そのペプチドが生体内の細胞内で発現という2条件を見出しました。この条件下では、抗原提示細胞の成熟化が起こり、これまでに反応しなかった新規がん特異的キラーT細胞を所属リンパ節で誘導できることを示しました。これらの配列はがんのフレームシフト変異による長鎖ペプチド産物に高頻度で含まれ、大腸がん患者データでもこの様ながん抗原を有する患者は良好な予後と相関しました。マウスモデルでは遠隔腫瘍抑制やPD-1抗体感受性増強が確認されました。本研究は、がん抗原同定を必要としない新しいアジュバント型免疫療法の概念を示すもので、免疫チェックポイント阻害薬に不応答性腫瘍を応答性へ転換できる可能性を持ちます。
本研究成果は、2025年12月5日に、国際学術誌「Journal of Experimental Medicine」にオンライン掲載されました。
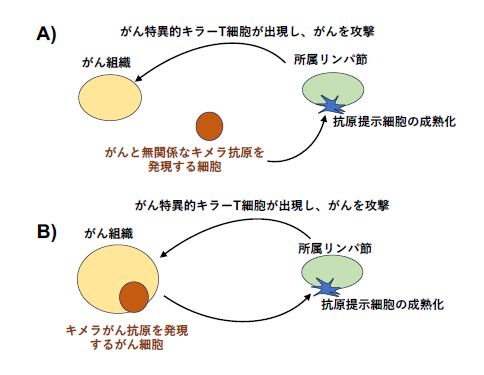
「今回の研究で、非特異的な抗原がどの様にして抗原特異的T細胞免疫反応を増幅するか明らかにすることができました。これは免疫学の根源的なメカニズムです。この発見をもとに、がん抗原の特異性に依存しないがん免疫治療の臨床応用開発をしたいと考えています。」(茶本健司)
【DOI】
https://doi.org/10.1084/jem.20250025
【KURENAIアクセスURL】
http://hdl.handle.net/2433/298521
【書誌情報】
Rongsheng Zhang, Rong Ma, Merrin M.L. Leong, Ian R. Watson, Kei Iida, Tomonori Yaguchi, Fumihiko Matsuda, Tasuku Honjo, Kenji Chamoto (2025). Chimeric MHC class I– and II–restricted non-self epitopes broaden antitumor T cell reactions. Journal of Experimental Medicine, 223, 2, e20250025.