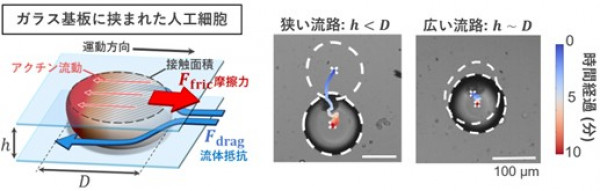
私たちの体の生体組織は細胞と細胞外基質から構成され、細胞間の隙間はコラーゲン線維などの細胞外基質で埋め尽くされた狭い空間です。この生体組織内を移動するガン細胞から白血球の運動に至るまで、単一細胞の自律運動では細胞内から細胞外への力伝達が不可欠です。そこでは、細胞内に網目状に張り巡らされたアクチン細胞骨格の収縮力が外部の基板に伝達され、細胞を前進させます。しかし、効率的な力伝達を可能にする仕組みは細胞の複雑さのため研究が困難でした。
宮﨑牧人 白眉センター特定准教授は、前多裕介 九州大学准教授、坂本遼太 同博士課程学生(現:イェール大学ポストドクトラルフェロー)、Ziane Izri 同学術研究員(現:ミネソタ大学ポストドクトラルフェロー)、島本勇太 国立遺伝学研究所准教授らと共に、生体内を移動するガン細胞を模した、自律的に運動する「人工細胞」を開発し、力伝達の仕組みを初めて明らかにしました。本研究チームは、脂質膜に囲まれた液滴のカプセルにアクチンを閉じ込めて単純化した人工細胞を作成しました。この人工細胞を2枚のガラス板に挟むと、アクチンの流れが人工細胞の表面とガラス基板の間に摩擦力を生み、自律的に運動できることを世界で初めて発見しました。さらに、狭い空間に拘束された運動を記述する新しい理論モデルを構築し、界面摩擦力と流体抵抗のバランスで運動速度が決まることを解明しました。本研究により、効率的な力の伝達に不可欠な物理的要因を明らかにしたことは、生体組織内を運動する細胞運動の力伝達メカニズムの理解に貢献する成果です。今後、ガン細胞の転移を抑えこむ方法論の開発の一助となり、狭い空間を移動するマイクロ・ロボットの設計などへの波及効果が期待されます。
本研究成果は、2022年7月20日に、科学雑誌「Proceedings of the National Academy of Sciences of the United States of America」で公開されました。
【DOI】
https://doi.org/10.1073/pnas.2121147119
【KURENAIアクセスURL】
http://hdl.handle.net/2433/278933
【書誌情報】
Ryota Sakamoto, Ziane Izri, Yuta Shimamoto, Makito Miyazaki, Yusuke T. Maeda (2022). Geometric trade-off between contractile force and viscous drag determines the actomyosin-based motility of a cell-sized droplet. Proceedings of the National Academy of Sciences, 119(30):e2121147119.