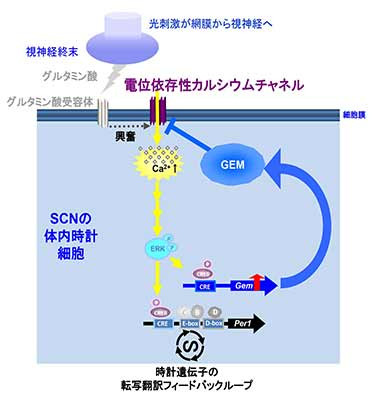
体内時計には、約24時間周期のサーカディアンリズムを生み出す仕組みだけでなく、このリズムのタイミングを環境の明暗変動に一致させるシステム(同調機構)があります。これは、眼で受けた光の明暗情報が視神経から体内時計中枢である視交叉上核に伝達され、この時刻を動かすことで行われます。哺乳類では、時刻を一度に3時間以上動かすことはできないことが知られています。しかし、その制限が作られる仕組みについては分かっていませんでした。
今回、松尾雅博 薬学研究科特定助教(現:滋賀医科大学)、岡村均 医学研究科研究員(京都大学名誉教授)、冨永恵子 大阪大学准教授らの研究チームは、光が神経活動を抑制する低分子量Gタンパク質Gemを誘導し、これが体内時計の細胞の活動を抑制し、過剰に動くことを防いでいることを明らかにしました。光刺激で時計細胞に発現したGemが、細胞が興奮するときに開く電位依存性カルシウムチャネル(VDCC)を抑制することで、細胞内へのカルシウムイオン流入量を減少させます。体内時計は、この仕組みをつかって、適切な時間の長さの時刻変動が起こるように調節していることが明らかになりました。
本研究成果は、2022年5月25日に、国際学術誌「Cell Reports」にオンライン掲載されました。
【DOI】
https://doi.org/10.1016/j.celrep.2022.110844
【KURENAIアクセスURL】
http://hdl.handle.net/2433/274091
【書誌情報】
Masahiro Matsuo, Kazuyuki Seo, Akiyuki Taruno, Yasutaka Mizoro, Yoshiaki Yamaguchi, Masao Doi, Rhyuta Nakao, Hiroshi Kori, Takaya Abe, Harunori Ohmori, Keiko Tominaga, Hitoshi Okamura (2022). A light-induced small G-protein gem limits the circadian clock phase-shift magnitude by inhibiting voltage-dependent calcium channels. Cell Reports, 39(8):110844.