2013年8月12日

左から阪井教授、田村 大阪大学ポストドクター
阪井康能 農学研究科教授、奥公秀 同助教、田村直輝 大阪大学蛋白質研究所ポストドクターらの研究グループは、メタノール資化性酵母Pichia pastorisより神経疾患に関連するPROPPINタンパク質の一つ、Atg18タンパク質を精製してその性質を調べ、Atg18がリン酸化型と脱リン酸化型の二種類を持ち、そのリン酸化調節がオルガネラの動態制御など、重要な生理機能を担っていることを明らかにしました。
Atg18は、酵母から高等生物にまで広く保存され、Atg18のリン酸化はヒトでも起きていることが予測されています。またAtg18は細胞内でさまざまな膜に結合したり離れたりしながら、オートファジー(細胞内の不要成分を自ら分解する働き)に関わっています。今回の研究は、どのようにしてAtg18のダイナミクスが調節されているかについて、生体膜側でなく、タンパク質のリン酸化が生体膜中に含まれるシグナルリン脂質PI(3, 5)P2への親和性を調節することにより行っていることを初めて示しました。
この研究成果は、米国科学誌「Journal of Cell Biology」誌のオンライン版(2013年8月12日午前9時 米国東部時間)に掲載されました。
背景
酵母から高等生物にまで広く保存されているタンパク質ファミリーPROPPINの一つAtg18は、細胞内で膜に結合したり離れたりしながら、オートファジーに関わっていることが知られていましたが、どのようにしてそのダイナミクスが調節されているかわかっていませんでした。最近、ヒトではPROPPINの一つであるWIPI4(Atg18のホモログ)がうまく働かなくなるとオートファジーが進まなくなり神経疾患(脳内鉄沈着神経変性症)を引き起こすこと (Nature Genetics 2013)、酵母やカビなどの真核微生物では植物葉上などの自然界やヒトや植物への感染時に増殖するときにオートファジーが必要で、地球温暖化に大きな影響を及ぼす炭素循環や食糧生産に重要な役割を果たしていること(PLoS One 2011; Plant Cell 2010)がわかっています。
研究成果
Atg18のリン酸化は、膜中に含まれるシグナルリン脂質への結合能を制御している
今回、メタノール資化性酵母Pichia pastorisより神経疾患に関連するAtg18タンパク質を精製してその性質を調べたところ、Atg18がリン酸化型と脱リン酸化型の二種類を持っていることがわかりました。Atg18のリン酸化はヒトでも起こっていることは予測されていますが、リン酸化型に比較すると脱リン酸化型Atg18では、生体膜中に含まれるシグナルリン脂質PI(3, 5)P2への親和性が高いことを明らかにしました。またAtg18のどこがリン酸化されるのか、そのアミノ酸残基と立体的な位置を決定し、膜との結合性を調べることにより、Atg18がリン酸化されると、どうしてPI(3, 5)P2を含む生体膜に結合しにくくなるのかについて、膜とタンパク質の立体構造から解明することができました。タンパク質のリン酸化は細胞内の情報伝達で重要な働きをしていることがわかっていますが、生体膜上のリン脂質の質や量でなく、タンパク質のリン酸化が生体膜との相互作用を、直接、調節していることを示した初めての例です。このように細胞内ではAtg18タンパク質のリン酸化を調節することで、生体膜への親和性を調節し、くっついたり離れたりしていることがわかりました。
Atg18のリン酸化調節が液胞膜への結合性、オルガネラ・ダイナミクスを制御している
Atg18のリン酸化制御が、酵母ではオルガネラの一つである液胞の形を制御していることを示しました。
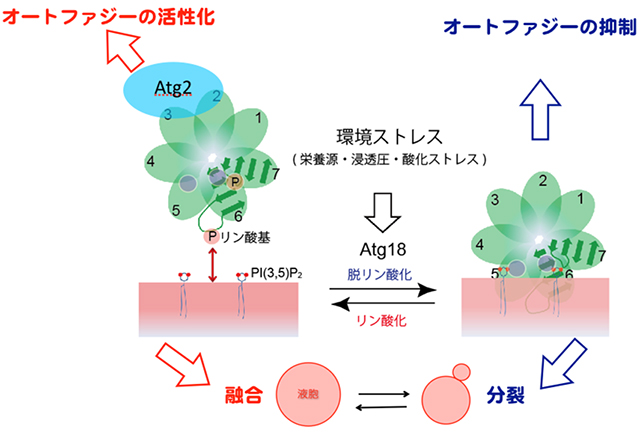
オートファジーの一種であるミクロオートファジーでは、液胞が別のオルガネラであるペルオキシソームを分裂しながら大きく包み込んでいきますが、Atg18を欠損させるとこのような液胞の形態変化が起きなくなります。また、高浸透圧条件では液胞は分裂によりその数を増やしていきますが、低浸透圧条件ではいくつかの液胞は融合しながら大きくなります。Atg18がリン酸化されるとAtg18は液胞膜から離れてオートファジーにおけるオートファゴソーム膜の形成に働きます。一方、Atg18が脱リン酸化されるとAtg18は液胞膜に結合して液胞の分裂を引き起こすことがわかりました。自然界にさらされる酵母は、Atg18のリン酸化を調節することで、液胞形態を変化させて浸透圧変化への対応とオートファジー活性の調節を行っていることがわかりました。同様のAtg18のリン酸化による調節がヒトの細胞でも起こっている可能性があります。
今後の展望
Atg18のリン酸化と細胞内で働く時の動態メカニズムが新たにわかったことで、今後、オートファジーやオルガネラの細胞内ダイナミクスが、どのように調節されているかについての理解が進むとともに、オートファジーやその調節がうまくいかないことに起因する疾患・植物病原菌の感染や共生の新たなメカニズムの解明、Atg18を含む疾患に関わるPROPPIN分子・Atg分子のリン酸化・脱リン酸化をターゲットとした新たな治療薬の開発が可能になったと考えられます。
書誌情報
[DOI] http://dx.doi.org/10.1083/jcb.201302067
[KURENAIアクセスURL] http://hdl.handle.net/2433/178058
Tamura Naoki, Oku Masahide, Ito Moemi, Noda Nobuo N., Inagaki Fuyuhiko, Sakai Yasuyoshi.
Atg18 phosphoregulation controls organellar dynamics by modulating its phosphoinositide-binding activity.
The Journal of Cell Biology, Published August 12, 2013.
- 京都新聞(8月13日 29面)に掲載されました。

