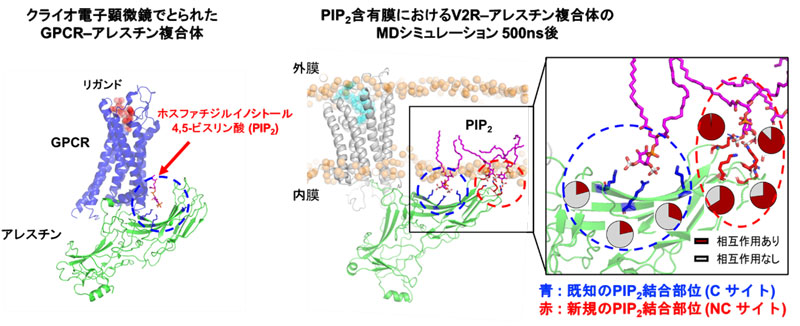
細胞はGタンパク質共役型受容体(GPCR)と呼ばれる細胞表面のセンサータンパク質を用いて、外界からの情報分子を細胞内に伝えます。この情報伝達の効率を調節する重要な仕組みの一つに、GPCRの細胞内への取り込み(内在化)による情報伝達の収束があり、アレスチンというタンパク質がその役割を担います。アレスチンがGPCRと結合する際に、機能性膜脂質であるPIP2が関わることが報告されていますが、その詳細な分子機構は不明な点が多く残されていました。
井上飛鳥 薬学研究科教授(兼:東北大学教授)、倉本律輝 東北大学博士課程学生らの研究グループは、アレスチンがPIP2と結合する新たな部位を見出し、この結合によってGPCRをPIP2が多く含まれる細胞膜の微小領域に集積させることで、GPCRの内在化を促進させることを明らかにしました。本研究の知見は特定のタンパク質と膜脂質を標的とした創薬の新たな可能性を提唱します。
本研究成果は、2025年8月6日に、国際学術誌「Nature Chemical Biology」に掲載されました。
【DOI】
https://doi.org/10.1038/s41589-025-01967-4
【KURENAIアクセスURL】
http://hdl.handle.net/2433/298032
【書誌情報】
Ritsuki Kuramoto, Tatsuya Ikuta, Carlo Marion C. Carino, Kouki Kawakami, Miisha Kushiro, Chihiro Watanabe, Yasunori Uchida, Mitsuhiro Abe, Yasushi Sako, Tomohiko Taguchi, Masataka Yanagawa, Asuka Inoue (2025). Membrane-domain compartmentalization of active GPCRs by β-arrestins through PtdIns(4,5)P₂ binding. Nature Chemical Biology, 21, 12, 1927-1937.