2012年1月16日
我々の脳が形づくられるためには、神経細胞のもととなる神経前駆細胞が生まれた場所から特定の領域に移動し、正しく配置される必要があります。神経細胞には主に興奮性神経細胞と抑制性神経細胞が存在し、これらのもととなる神経前駆細胞は異なる場所で作られます。興奮性神経前駆細胞に比べ、抑制性神経前駆細胞はより長い距離を、より速い速度で移動する必要があるため、特有の細胞内メカニズムを備えていると考えられます。白血球など他の細胞と異なり、神経前駆細胞は移動方向に長い先導突起を伸ばし、細胞体は先導突起を追いかけるようにリズミカルな「跳躍運動」を示します(図)。我々の体内ではアクチン細胞骨格という細胞の骨組みとなるたんぱく質が組み立てられたり(重合)、バラバラにされたり(脱重合)することで細胞の形態形成や運動が調節されていますが、神経前駆細胞における跳躍運動がどの様なメカニズムで引き起こされているのかは明らかにされていません。
今回、成宮周 医学研究科教授(神経・細胞薬理学)、古屋敷智之 同助教、篠原亮太 同大学院生(博士課程)らの研究グループは、細胞内でアクチン細胞骨格の重合に関わるたんぱく質「mDia」分子を欠損したマウス(mDia欠損マウス)を解析しました。彼等はこの変異マウスでは興奮性神経細胞は正常に配置されますが、抑制性神経前駆細胞の細胞体の跳躍運動が著しく減少しており、脳内で正しく配置されないことを発見しました。また、細胞体の跳躍運動において、mDiaは細胞の後部に一時的に集まり、局所的にアクチン細胞骨格を重合することにより、細胞体を後部から押し出すことが明らかとなりました(図)。 これまで神経前駆細胞の移動メカニズムの研究の多くは興奮性神経前駆細胞を対象にして行われてきましたが、今回発見されたメカニズムは抑制性神経細胞に特有であり、速い神経前駆細胞の移動を可能にするためのメカニズムであると考えられます。
抑制性神経細胞の異常は、てんかん、自閉症、統合失調症など様々な精神疾患に関わることが示唆されています。また、mDiaにはヒトの相同遺伝子が存在し、その異常は自閉症の発症と関連があることから、今回の研究成果は、それらの疾患発症メカニズムの解明にも役立つと期待されます。
本研究成果は、竹林浩秀 新潟大学教授、渡辺啓介同助教、澤本和延 名古屋市立大学教授、金子奈穂子 同助教、清成寛 理化学研究所CDB研究員との共同研究で得られ、2012年1月15日(米国東部時間)発行の「NatureNeuroscience」オンライン版に掲載されました。
【論文情報】
"A role for mDia, a Rho-regulated actin nucleator, in tangential migration of interneuron precursors"(抑制性神経前駆細胞の tangential migration におけるRho標的アクチン重合因子mDiaの役割)
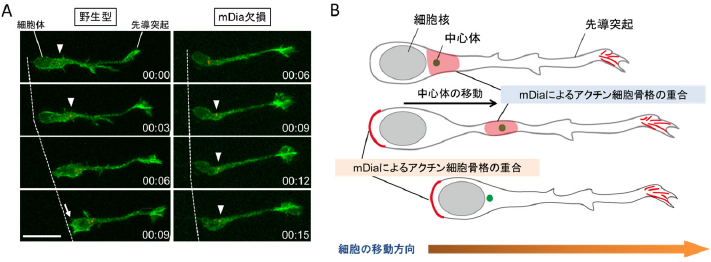
- 図.抑制性神経前駆細胞の移動におけるmDiaの役割
A.正常な細胞(野生型)では、細胞体移動時に一時的なアクチン細胞骨格の重合(緑色)が細胞体後部で観察される(矢印)。一方、mDia欠損細胞では、細胞体後部のアクチン線維の集積と細胞体の移動が起こらない。矢頭は中心体(赤色)の位置を示す。
B.モデル図。mDiaは細胞体後部に一時的に集まり、局所的にアクチン細胞骨格を重合することで細胞体を前方に押し出す。
本研究への支援
本研究成果は、以下の事業・研究領域・研究課題によって得られました。
- 科学研究費補助金 基盤研究(S)
研究課題名:「個体での組織構築・恒常性におけるRho-mDia経路の役割」
研究代表者:成宮 周(京都大学 大学院医学研究科 教授)
研究期間:2011年4月~2014年3月 - 戦略的創造研究推進事業(CREST)
研究領域:「炎症の慢性化機構の解明と制御に向けた基盤技術の創出」
研究課題名:「プロスタグランジンを引き金とする炎症慢性化機構の解明」
研究代表者:成宮 周(京都大学 大学院医学研究科 教授)
研究期間:2011年4月~2016年3月
関連リンク
- 論文は以下に掲載されております。
http://dx.doi.org/10.1038/nn.3020
http://hdl.handle.net/2433/152361 (京都大学学術情報リポジトリ(KURENAI)) - 以下は論文の書誌情報です。
Shinohara R, Thumkeo D, Kamijo H, Kaneko N, Sawamoto K, Watanabe K, Takebayashi H, Kiyonari H, Ishizaki T, Furuyashiki T, Narumiya S. A role for mDia, a Rho-regulated actin nucleator, in tangential migration of interneuron precursors. Nat Neurosci. 2012 Jan 15. doi: 10.1038/nn.3020.
- 京都新聞(1月17日 27面)および科学新聞(2月10日 2面)に掲載されました。

