2014年1月29日

左から片平教授、古川特別研究員
片平正人 エネルギー理工学研究所教授と古川亜矢子 日本学術振興会特別研究員らは、医学部、サントリー生命科学財団、セルフリーサイエンス社、横浜市立大学との共同研究によって、抗エイズウイルス活性を有するヒトのAPOBEC3G(A3G)タンパク質の酵素反応を、NMR(核磁気共鳴)法によってリアルタイムで追跡し、定量的に解析することに成功しました。これによって、A3Gタンパク質がエイズウイルスの遺伝子を効率的に破壊する仕組みが明らかになりました。
本研究成果は、2014年1月29日にドイツ科学誌「Angewandte Chemie International Edition」のオンライン版に掲載されました。また同誌のVery Important Paper (VIP)に選定されました。
背景
ヒトのAPOBEC3G(A3G)タンパク質は、エイズウイルスの遺伝子のシトシン塩基を脱アミノ化してウラシル塩基に変換することでウイルスの遺伝情報を破壊し、抗エイズウイルス活性を示します(図1)。A3GはまずウイルスDNAに非特異的に結合し、その後DNA上をスライディングして標的となるシトシンに到達し、酵素反応を引き起こします。また酵素反応は、ウイルスDNA上の複数の標的シトシンにおいて同時に並行して進行します。ミカエリス-メンテン法などの従来の酵素反応の解析手法ではこのような複雑な系を解析することができず、A3Gタンパク質が働く仕組みは謎に包まれていました。
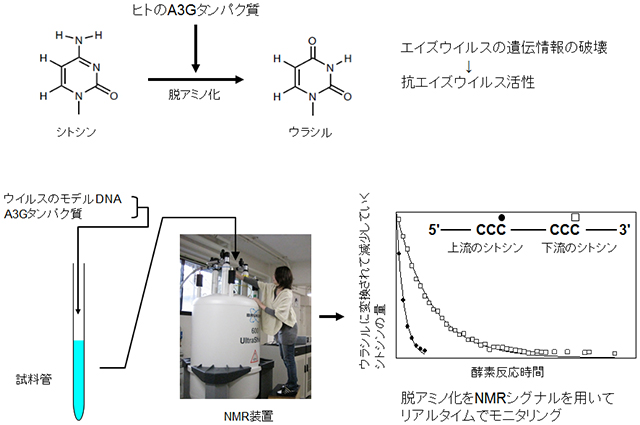
図1:(上)A3Gタンパク質は、エイズウイルスのDNAのシトシン塩基に作用してウラシル塩基に変換することでウイルスの遺伝情報を破壊し、抗エイズウイルス活性を示します。(下)ウイルスのモデルDNAとA3Gタンパク質を混ぜてNMR装置にセットすることで、DNA上の複数箇所で同時並行に進行する酵素反応を、NMRシグナルを用いてリアルタイムでモニタリングすることに成功しました。
研究手法・成果
ウイルスのモデルDNAとA3Gタンパク質を試料管に入れ、これをNMR装置にセットしました。そしてDNA上の複数のシトシンで同時並行に進行する塩基変換反応を、各シトシンに由来するNMRシグナルを別個に観測することで、リアルタイムでモニタリングすることに成功しました(図1)。次にA3GのDNAへの非特異的な結合と結合後のDNA上でのスライディングを考慮した反応モデルを構築し、上記で得られた実験結果を定量的に解析しました。この結果A3Gは上流方向にスライディングしながら標的シトシンに到達した際には、下流方向にスライディングしながら到達した際より、脱アミノ化反応の酵素活性が高いことが分かりました(図2)。上流に近い標的シトシンほど脱アミノ化されやすいことがこれまで観測事実として知られていましたが、酵素活性がスライディングの方向に依存するという今回得られた知見により、このことを合理的に説明することが初めてできるようになりました。また脱アミノ化による遺伝情報の破壊が既に為された直近の部位には、A3Gはもはやあまり作用しないことも分かりました。これは、エイズウイルスのDNA上の広い範囲で効率的に遺伝情報の破壊を行うのに適した性質だと考えられます。このようにNMRシグナルを用いたリアルタイムモニタリングによって、これまで不明であったA3Gタンパク質の動作機構が解明されました。
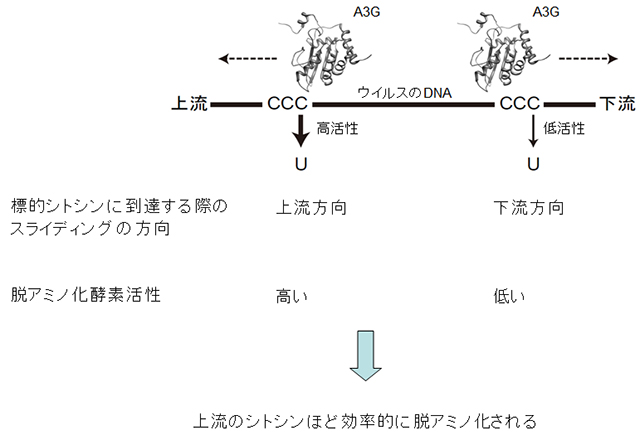
図2:リアルタイムモニタリングの結果を解析した結果、A3GはDNA上を上流にスライディングしながら標的シトシンに到達した際、下流にスライディングしながら到達した際より、脱アミノ化反応の酵素活性が高いことが分かりました。上流のシトシンほど脱アミノ化され易いことがこれまで観測結果として知られていましたが、今回得られた知見によってこのことを初めて合理的に説明することが可能となりました。
波及効果
A3Gタンパク質の抗エイズウイルス活性の根幹である脱アミノ化反応の動作機構が解明されたことで、A3Gを活用した抗エイズウイルス薬の創製の活性化が期待されます。また今回開発したNMRシグナルを用いた反応のリアルタイムモニタリングと定量解析の手法は、同時並行的に進行する他の複雑な酵素反応や生体内カスケード反応の解析にも応用できます。またNMRシグナルを用いたリアルタイムモニタリング法は、バイオマスを微生物によって分解することでエネルギーや化成品等の有用物質を獲得する際にも、時々刻々変わる物質群の動態を一網打尽に解析することができ、役立つと考えられます。
今後の予定
本研究グループは以前、A3Gの立体構造の決定にも成功しています(EMBO J., 2009)。これをA3Gの動的な側面に関する今回の知見と合わせることで、A3Gを活用した新規の抗エイズウイルス薬創製の基盤を確立していきたいと考えています。またNMRシグナルを用いたリアルタイムモニタリング法を、バイオマスから有用物質を獲得するのに活用することを始めており、この進展を目指します。
用語解説
NMR(核磁気共鳴)装置
MRI(核磁気共鳴画像法)と同様な原理に基づく分析装置
書誌情報
[DOI] http://dx.doi.org/10.1002/anie.201309940
[KURENAIアクセスURL] http://hdl.handle.net/2433/199659
Ayako Furukawa, Kenji Sugase, Ryo Morishita, Takashi Nagata, Tsutomu Kodaki, Akifumi Takaori-Kondo, Akihide Ryo, Masato Katahira
"Quantitative Analysis of Location- and Sequence-Dependent Deamination by APOBEC3G Using Real-Time NMR Spectroscopy"
Angewandte Chemie International Edition Early View Article first published online: 29 Jan 2014

