2013年11月4日

左から原助教、土屋助教
原英樹 医学研究科助教、土屋晃介 同助教、河村伊久雄 同准教授、光山正雄 同名誉教授(現 総合生存学館特定教授)らの研究グループは、自然免疫機構による生体の炎症応答に重要なインフラマソームを構成するASC分子の活性化機構を解明し、ASCの特定部位のリン酸化がインフラマソームの制御に必須であることを見い出しました。
本研究成果は2013年11月3日13時(米国東部時間)に米国科学誌「Nature Immunology」のオンライン版に公開されました。
背景
インフラマソームとは
自然免疫は下等生物から高等生物まで保存された生体防御機構であり、多数のパターン認識受容体が自然免疫応答の中心的役割を担っています。NLRP3やAIM2、NLRC4などのパターン認識受容体は、特定の刺激因子(アゴニスト)を認識すると構造変化を起こしてASCやカスパーゼ-1などのタンパク質と介合し、インフラマソームと呼ばれるタンパク複合体を形成します(図1)。インフラマソームではタンパク分解酵素の一種であるカスパーゼ-1が活性化され、活性型カスパーゼ-1がインターロイキン-1などの炎症性サイトカインの成熟化・分泌を誘導することで炎症が起こります。
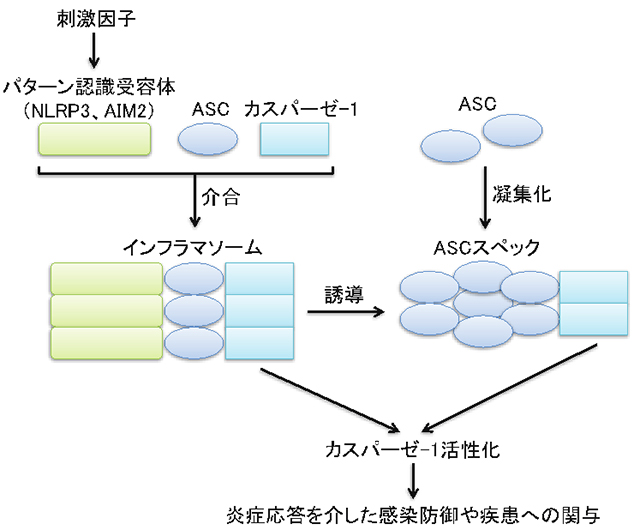
図1:インフラマソームおよびASCスペックの構造と形成過程
インフラマソームの生理的役割および疾患との関連
インフラマソームの形成は病原微生物の感染によって誘導され、それに基づく炎症応答は多くの場合、感染防御に有効であり、インフラマソームは腸内細菌叢の制御および腸管上皮バリアの保護に働き、腸管の恒常性維持に寄与するとも考えられています。一方、インフラマソームが示す負の側面も知られており、刺激因子の種類によっては、過剰なインフラマソーム形成が不適切かつ持続した炎症を惹起し、動脈硬化、痛風、2型糖尿病、アルツハイマー病などの各種疾患の発症に関わります。また、ある種の自己炎症疾患の発症はインフラマソーム構成タンパクの突然変異が関与することも示唆されています。そのため、インフラマソームの形成または活性の制御機構を解明することは、病態機構の理解を深め、診断や治療へ貢献するものと期待されます。
ASCスペックについて
インフラマソーム構成タンパクであるASCは、インフラマソームにおいては受容体とカスパーゼ-1の介合を助ける連結因子として働きますが、インフラマソームが形成される際に自身が凝集化して別のタンパク複合体(以降ASCスペックと呼ぶ)を形成します(図1、図2)。ASCスペックは、インフラマソームと同様にカスパーゼ-1を呼び寄せてカスパーゼ-1活性化の場として働くことから、インフラマソームを介した炎症応答で重要な役割を果たしていますが、ASCスペックの形成がどのような機序で誘導されるかはこれまで明らかではありませんでした。
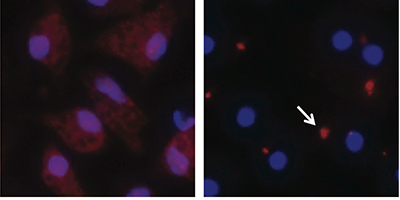
図2:ASCスペックの観察
ASCと核をそれぞれ赤色および青色の蛍光色素で染色し、蛍光顕微鏡で観察した。左に未処理マクロファージ、右にnigericinで刺激したマクロファージを示す。ASCは未処理マクロファージでは細胞内に遍在するが、nigericin刺激によってNLRP3インフラマソームが活性化されると凝集化してASCスペックを形成する(1例を矢印で示す)。
研究手法・成果
本研究において研究グループは、インフラマソームの形成や活性に関わるシグナル伝達経路を探索する目的で、各種シグナル阻害剤のインフラマソームへの影響を調べました。その結果、キナーゼであるSykおよびJNKが、NLRP3インフラマソームおよびAIM2インフラマソームを介したカスパーゼ-1活性化や炎症性サイトカインの産生に関わることがわかりました。そこで、なぜSykとJNKがインフラマソームの活性に関わるか調べました。さまざまな可能性を検討したところ、ASCスペックの形成がこれらのキナーゼに依存していることがわかりました。すなわち、SykとJNKはASCスペックの形成を制御することで、インフラマソームを介した炎症応答に寄与することが示唆されました。次にSykとJNKがどのような機序でASCスペックの形成を制御するかを検討しました。SykとJNKがキナーゼであることから、インフラマソーム構成タンパクのリン酸化が関与する可能性を考え、インフラマソーム形成時にリン酸化されるタンパクを探したところ、ASCがSykおよびJNKに依存してリン酸化されることが明らかになりました。また、ASCの144番目のチロシン残基(Y144)がリン酸化部位であることを同定することが出来ました。さらに、Y144の変異体を用いた実験により、同アミノ酸残基がASCスペックの形成や炎症性サイトカインの産生誘導に重要であることもわかりました。これらの実験結果から、SykおよびJNKに依存したASCの特定のチロシンリン酸化が、ASCスペックの形成に重要な役割を果たし、インフラマソームを介した炎症応答の誘導に働くことが示されました(図2)。次に、明らかになったSykおよびJNKのインフラマソームへの関与が生体内で再現できるか、マウスの腹膜炎モデルを用いて検討しました。マウスの腹腔に尿酸結晶を投与するとインフラマソーム依存的に好中球浸潤が起こることが知られています。しかし、SykまたはJNKの非存在下では尿酸結晶による好中球浸潤の誘導が有意に減少していたため、これらのキナーゼは生体内においてもインフラマソームを介した炎症応答の誘導に働くことが確認されました。
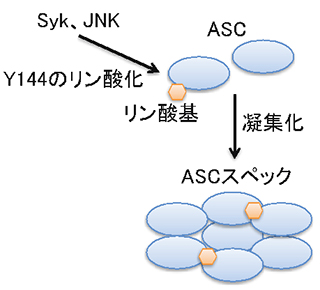
図3:リン酸化によるASCスペック形成の制御
波及効果
これまで、ASCスペックの形成は単純にASC分子の凝集現象と考えられてきましたが、キナーゼによるASCのリン酸化がその過程に重要な役割を果たすことが今回の研究で初めて明らかになりました。キナーゼによるタンパクのリン酸化反応は化合物による抑制が比較的容易であることから、ASCのリン酸化を特異的に阻害する化合物の探索、設計により、インフラマソームを介した炎症応答の制御、ひいてはインフラマソーム関連疾患の治療に応用することも期待できると考えられます。
今後の予定
今後、ASCのリン酸化がASCスペックの形成に働く、さらに詳細なメカニズムを明らかにする必要があります。また、自己炎症疾患のモデルマウスなどを用い、SykやJNKの阻害が実際に症状を緩和するか否かを確認する必要があります。
用語解説
インフラマソーム
多様な刺激因子に応じて細胞内に形成されるタンパク複合体であり、特定のパターン認識受容体、ASC、カスパーゼ-1で構成される。インフラマソームではカスパーゼ-1分子間の近接化が起こることでカスパーゼ-1が活性化される。
ASC
Apoptosis-associated speck-like protein containing caspase recruitment domainの略。ASCはインフラマソームを構成するタンパク質の一つであり、受容体とカスパーゼ-1の介合を助ける連結因子として働く。また、ASCはインフラマソームが形成される際に凝集化してASCスペックと呼ばれるタンパク複合体を形成する。ASCスペックはインフラマソームと同様にカスパーゼ-1を呼び寄せてカスパーゼ-1活性化の場として働く。
NLRP3、AIM2、NLRC4
これらはパターン認識受容体であり、それぞれ異なる刺激因子を認識する。その後、構造変化を起こしてASCやカスパーゼ-1と介合し、インフラマソームを形成する。各インフラマソームの名前は、含まれるパターン認識受容体をもとに名付けられる(NLRP3インフラマソームなど)。
カスパーゼ-1
システインプロテアーゼ(タンパク分解酵素)の一種である。不活型として合成されるが、インフラマソームが形成されると、そこで自己分解性に活性化される。活性型カスパーゼ-1はシステインプロテアーゼとして複数の基質を分解できる。特に、未熟型インターロイキン-1βを分解することで成熟化させ、成熟型インターロイキン-1βは強力な炎症性サイトカインとして働く。
書誌情報
[DOI] http://dx.doi.org/10.1038/ni.2749
[KURENAIアクセスURL] http://hdl.handle.net/2433/179525
論文名
"Phosphorylation of the adaptor ASC acts as a molecular switch that controls the formation of speck-like aggregates and inflammasome activity"
ジャーナル名
Nature Immunology Advanced Online Publication Published online 03 November 2013
著者
Hideki Hara1, Kohsuke Tsuchiya1, Ikuo Kawamura1, Rendong Fang1, Eduardo Hernnandez-Cuellar1, Yanna Shen1,2, Junichiro Mizuguchi3, Edna Schweighofer4, Victor Tybulewicz4 and Masao Mitsuyama1
1 医学研究科
2 天津医科大学
3 東京医科大学
4 MRC国立医学研究所
- 日刊工業新聞(11月6日 23面)、読売新聞(11月4日 2面)および科学新聞(11月29日 4面)に掲載されました。

