2013年10月25日

左から亀井助教、ステファン助教、北川拠点長・教授、古川准教授
北川進 物質-細胞統合システム拠点(iCeMS=アイセムス)拠点長・教授、古川修平 同准教授、ステファン・ディーリング 同助教らの研究グループは、一酸化窒素(NO)を光により自在に取り出すことが可能な多孔性構造体の開発に成功しました。さらに、亀井謙一郎 同助教らのグループと協力し、この材料を細胞培養基板に埋め込むことで、細胞の狙った場所をNOで刺激することに成功しました。
本成果により、NOが直接関与しているとされる血管拡張、記憶形成、免疫、代謝などの生物学・医学分野において、細胞の中でのNOの役割解明に寄与することが期待されます。
本成果は2013年10月25日10時(日本時間25日18時)に英国オンライン科学誌「Nature Communications」で公開されました。
背景
ガス状分子である一酸化窒素(以下「NO」とする。)は私たちの身体の中で作り出され、細胞間のコミュニケーションを調整する分子として知られています(情報伝達物質)。特に1987年にNOが血圧に応じて血管を弛緩する主要な因子(血管内由来弛緩因子:EDRF)として同定されて以来、中枢神経系などにおける情報伝達作用などさまざまな生理的作用を持っていることが明らかとなってきました。例えば、狭心症などの治療に使用されることでよく知られる血管拡張薬ニトログリセリンは、体内で加水分解・還元反応を介してNOになることによって、その効果を示します。一方で、一酸化窒素は毒性を持つガスとしても知られており、高濃度のNOを生物が吸収すると死に至り得ます。細胞に対しても同様、マクロファージと呼ばれる細胞は外敵(細菌、バクテリアなど)を殺すために、NOを放出するシステムを持っています。このようにNOは生物学ではもちろん、医学的にも重要な分子であり、その驚くべき生物学的機能の発見に対し、1998年にノーベル生理学・医学賞が授与されました。しかしながら、細胞内でどのような分子的メカニズムでNOが作用しているのかという謎は未だ完全には解明されていません。その理由には、NOはガス状分子であるため同じ場所に留まることができず(拡散が速く)、取り扱いが非常に困難なことが挙げられます。そこで、細胞内という非常に小さな領域で、NOの濃度を自在に制御できる材料の開発が待ち望まれてきました。
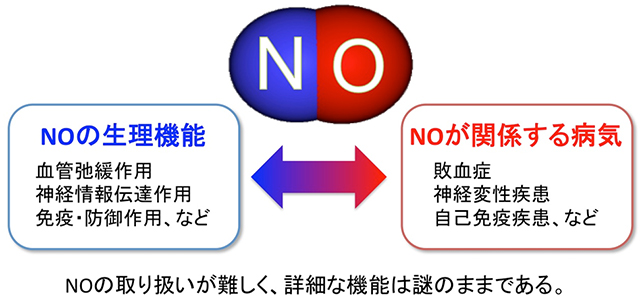
図1:一酸化窒素(NO)の生理学的役割の概要
一方で、多孔性金属錯体(PCP)とよばれる金属イオンと有機物からなる、極めて均一なナノサイズの細孔を持つ多孔性物質が近年注目を集めています。この結晶性化合物は、細孔のサイズや特性を変えることができるため、目的に応じた設計が可能であり、さまざまな分子(特にガス分子)をその細孔中に効率的に取り込むことができます。その性質を活かして、エネルギー燃料であるメタンや水素ガスの大量吸蔵や分離、二酸化炭素の大気中からの分離などへの応用が期待されており、高い注目を集めています。これらの機能は「ガスが細孔の中に入ってくる」現象であり、これまではこの制御を行う研究が主になされてきました。本研究グループでは、このPCPにNOを取り込ませ、必要な時に必要なだけ取り出すことができる材料が開発できれば、細胞内におけるNOの濃度調整ができるのではないかと考えました。しかし、そのためには「ガスが細孔から出てくる」というこれまでとは全く逆の現象を制御する必要があります。そこで本研究グループでは、新しいPCPの合成に取り組みました。
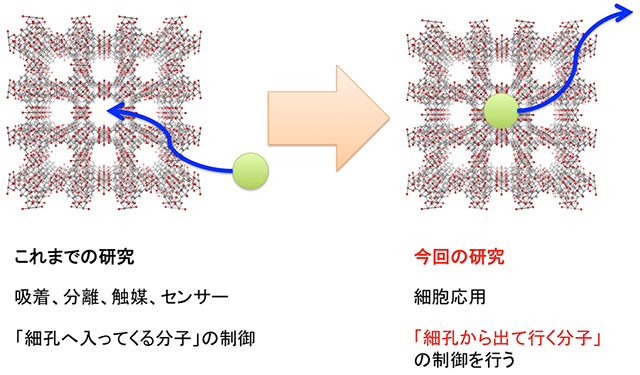
図2:これまでのPCPの「ガスが細孔の中に入ってくる」現象を制御する概念と、今回取り組んだ「ガスが細孔から出て行く」現象を制御する概念の違い。
研究内容と成果
本研究では、PCPに閉じ込めたNOを光照射によってのみ取り出すことに成功し、さらに細胞培養基板にPCP結晶を埋め込むことで、レーザー光で狙った場所でのみNOを取り出し、生きた細胞に取り込むことに成功しました。
細胞実験を行う室温・大気圧中ではNOはガス状の分子であるため、PCPの細孔で単純に取り込むことはできず、PCPと強い化学結合を持たせる必要があります。そこで、本研究グループは、NOをニトロ基(—NO2)として共有結合的にPCPの骨格に固定しました。具体的には、イミダゾールと呼ばれるPCPを構築する有機化合物にニトロ基を導入したニトロイミダゾールを用いて亜鉛イオンとともに反応させることで、図3に示したようなPCPを合成しました。ここではこのPCPをNOF-1と呼ぶことにします(NOF:Nitric Oxide Frameworkの略称)。このNOF-1に紫外光を当てると、ニトロ基が分解され、NOが放出されることが確認されました。実際に紫外光の照射を止めると、数秒のうちにNOの放出はなくなり、光のON/OFFでNOの放出を制御できることがわかりました。さらに時間あたりの放出量は、当てる光の強度を変えることで調整できることもわかりました。
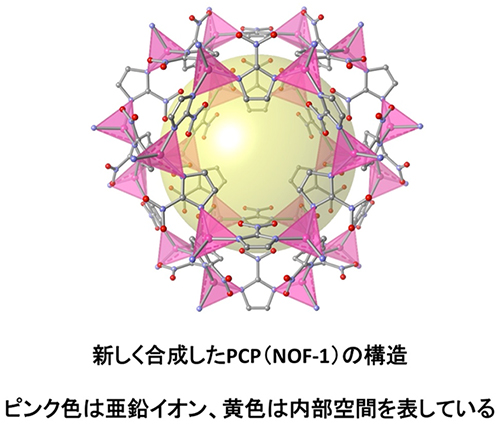
図3:NOF-1の結晶構造解析による分子構造
次に、NOF-1を細胞実験に応用するために、図4に示すような細胞培養基板を作成しました。まず、ガラス基板上にNOF-1結晶をコーティングした後、生体適合性の高いシリコンゴムPDMSをさらに上からコーティングしました。このPDMSはガス透過性が高いことでも知られており、NOF-1結晶から放出されたNOガスを妨げることなく、速やかにPDMS膜を透過することができます。細胞培養を行うために、このNOF-1を用いた細胞培養基版を70%エタノールで滅菌した後、細胞接着・増殖を促すマトリゲルをコーティングしました。
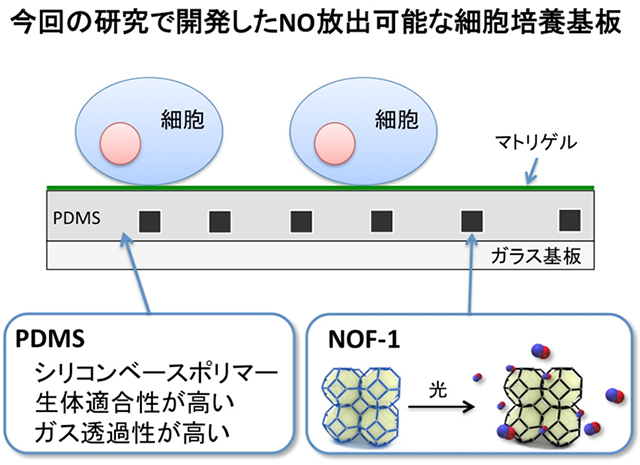
図4:NOF-1結晶を用いた細胞培養基板
この細胞培養基板中に埋め込まれたNOF-1結晶にのみ、顕微鏡下でレーザーを当てることで局所的にNOを放出することができます。また、この基板の上にNOと反応すると緑色に発色する蛍光分子を入れたHEK293細胞と呼ばれる細胞を培養しました。これにより、図5に示すように、狙った場所にレーザー光を当てることで、自在にNOを放出し、局所的に細胞刺激を行うことができる全く新しい手法の開発に成功しました。
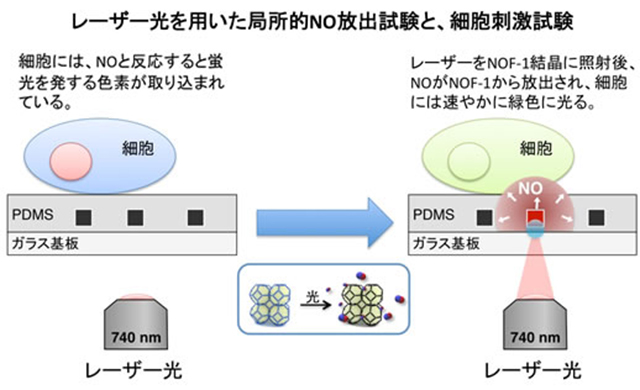
図5:細胞を用いた実験概要。細胞にはNOと反応すると蛍光を発する指示薬が導入されている。NOと反応した細胞のみ蛍光を発するので、局所的なNO放出、および細胞刺激を観察することができる。
今後の期待
今回、本研究グループが開発した手法は、光によりNOを取り出すことができるPCPを開発し、それをさらに培養基板へ埋め込むことで、実際に細胞生物学へ応用することが可能になりました。この細胞培養基板は、他にも数多くの細胞種(ES/iPS細胞、神経細胞など)の培養・刺激試験への応用が可能です。今後は、さまざまな細胞へ応用することで、未だ謎のままであるNOの細胞内での役割を解明していく予定です。
用語解説・注釈
一酸化窒素
化学式で表すと「NO」となる、常温・大気圧条件下ではガス状の分子。1987年に血管弛緩を担う因子として同定されて以来、神経・幹細胞などでのさまざまな生理活性を持つことが明らかになってきている。その反面、神経変性性疾患などへの関与も報告され、NOの作用機構解明が今後の薬剤開発などにおいて重要となっている。
多孔性構造体
多数の微細な孔を持つ物質。吸着材、分離材や触媒などに利用される。
1998年のノーベル生理学・医学賞
1987年にNOが血管弛緩を担う因子であると同定し、さらに細胞シグナル伝達への関与を明らかにした功績を評して、ムラド教授(米国ジョージ・ワシントン大学)、ファーチゴット教授(米国ニューヨーク州立大学、故人)、イグナロ教授(米国カリフォルニア大学ロサンゼルス校)に授与された。
多孔性金属錯体(PCPもしくはMOF)
金属イオンと有機物がジャングルジム状に組み上がった金属錯体結晶。本質的に内包するナノサイズの細孔を利用した、ガス貯蔵・ガス分離・触媒・センサーなど幅広い分野での応用が期待されている化合物群
書誌情報
[DOI] http://dx.doi.org/10.1038/ncomms3684
論文タイトル
"Localized cell stimulation by nitric oxide using a photoactive porous coordination polymer platform"
著者
Stéphane DIRING, Dan Ohtan WANG, Chiwon KIM, Mio KONDO, Yong CHEN, Susumu KITAGAWA, Ken-ichiro KAMEI*, Shuhei FURUKAWA*
掲載誌
Nature Communications 4, Article number: 2684 Published 25 October 2013
- 京都新聞(10月26日 29面)、中日新聞(10月26日滋賀版 3面)、日刊工業新聞(10月28日 17面)および読売新聞(1月20日 19面)に掲載されました。

