2013年3月12日

左から楠見教授、永田特定拠点助教、植田教授
植田和光 物質-細胞統合システム拠点(iCeMS=アイセムス)教授、永田紅 同特定拠点助教、楠見明弘 同教授らの研究グループは、善玉コレステロール(HDL)の産生に必須である膜タンパク質ABCA1(ATP-binding cassette protein A1)を1分子レベルで観察し、HDLができる最初の段階を可視化することに世界で初めて成功しました。
健康診断の血液検査での指標として用いられているように、血中HDL量の多い人は動脈硬化症を発症しにくいことがわかっています。しかし、アポリポタンパク質とコレステロールの複合体であるHDLがどのようなメカニズムでできるかは明らかになっていませんでした。
本研究では、細胞内の過剰なコレステロールを排出する能力をもつABCA1が、細胞膜上で二量体を形成することが、HDLができる過程で重要であることが初めて示されました。この結果は、HDLができるメカニズムを解き明かすうえで重要であり、本成果をさらに発展させることで動脈硬化症の予防や治療法の開発につながると期待されます。
本研究成果は、米国東部時間3月11日に米科学誌「アメリカ科学アカデミー紀要(Proceedings of the National Academy of Sciences of the United States of America)」電子版に公開されました。
背景
コレステロールは細胞膜の主要な構成成分として、またホルモンの前駆体として、生体にとって重要な成分ですが、細胞内に過剰に蓄積すると害を及ぼし、動脈硬化の原因となります。したがって、体内のコレステロール恒常性を維持することは重要です。
血液検査の結果で目にすることの多い「善玉コレステロール(HDL)」は、実はコレステロールだけから成っているのではなく、コレステロールやリン脂質などの脂質を2分子のアポリポタンパク質と呼ばれるタンパク質が束ねた、脂質とタンパク質の複合体です。全身の細胞でコレステロールが過剰になると、コレステロールは細胞膜上で働くABCA1という膜タンパク質の働きによって細胞外へと運び出され、血中を流れているアポリポタンパク質へと受け渡されます。HDL複合体は肝臓へ運び戻され、体内のコレステロールの恒常性が維持されます(図1)。
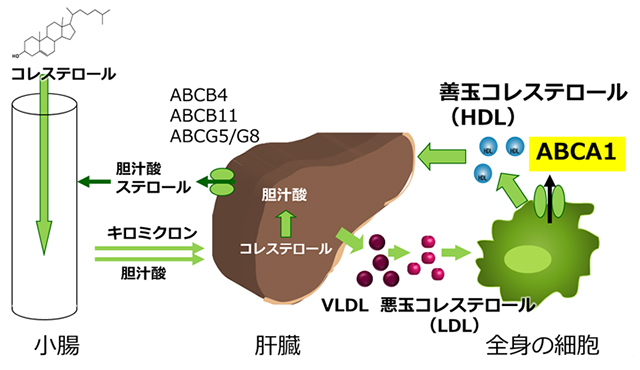
図1:体内のコレステロールの循環
ABCA1は、血中HDLが消失する遺伝病であるタンジール病の原因遺伝子として1999年に発見され、HDL形成に必須であることが明らかにされました。ABCA1は、ATPのエネルギーを利用してさまざまな物質を輸送するABCタンパク質というトランスポーターの一種であることから、コレステロールがABCA1によって動かされ、HDLができると予想されていましたが、どのようなメカニズムでできるかはわかっていませんでした。
本研究では、細胞膜上のABCA1とアポリポタンパク質を1分子レベルで観察し、HDLができる初期段階を可視化することに成功しました。それによって、HDLができる過程でABCA1が一時的に二量体となって、アポリポタンパク質にコレステロールを受け渡すことが明らかになりました。
研究内容と成果
今回、本研究グループは全反射照明蛍光顕微鏡を用い、細胞膜上のABCA1分子(緑色蛍光タンパク質=GFPを融合し、蛍光観察できるようにしたABCA1-GFP分子)の挙動を1分子レベルで観察しました。通常、一般的な膜タンパク質は細胞膜平面上を拡散によって動き回りますが、興味深いことに、アポリポタンパク質の非存在下では、ABCA1分子の多く(約70%)は一箇所に静止したままであるという特徴的な挙動を示しました(図2)。したがって、ABCA1には分子を細胞膜上で不動化している何らかの機構があることが予想されました。詳しく調べると、この静止しているABCA1分子の約90%は二量体(二つのABCA1分子がまとまった状態)を形成していることが明らかになりました。
一方、HDLを産生する機能を持たない変異型ABCA1分子は二量体化せず、単量体の状態のままで細胞膜上を拡散していました(図2)。したがって、コレステロールを動かす能力のあるABCA1は、コレステロールの受け取り手であるアポリポタンパク質がやって来る前の段階では、二量体の形となって細胞膜上に静止していることがわかりました。
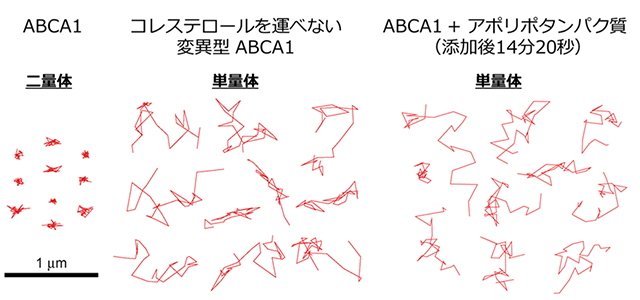
図2:ABCA1分子の細胞膜上での代表的な1秒間の軌跡
本研究グループは、ABCA1は細胞膜中のコレステロールを動かして自身の分子内に溜め込み、二量体化して、コレステロールの受け取り手であるアポリポタンパク質の接近に備えてスタンバイしているものと考えています。
- ABCA1は細胞膜上で二量体を形成して静止し、アポリポタンパク質がやってくるのを待っている
体内では、コレステロールの受け取り手であるアポリポタンパク質が血中を流れています。そこで、細胞の外からアポリポタンパク質を添加する実験を続いて行いました。培養培地にアポリポタンパク質を添加すると、面白いことに、二量体となっていたABCA1が単量体に解離し、細胞膜上を拡散し始める様子が観察されました(図2)。この結果より、ABCA1からアポリポタンパク質へとコレステロールが受け渡された結果、善玉コレステロールHDLが形成され、一方、溜め込んでいたコレステロールを放出したABCA1は単量体に戻ってまたコレステロールを集めにかかるというサイクルがあることがわかりました。本研究によって、善玉コレステロールHDLの産生のためには、このようなABCA1の二量体と単量体の相互変換が繰り返されていることが初めて明らかになりました(図3、4)。
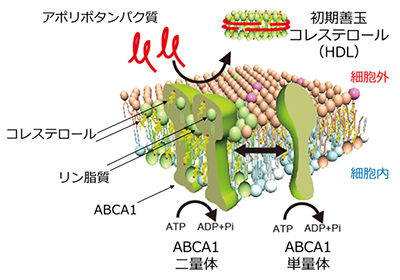
図3:ABCA1による善玉コレステロール産生モデル
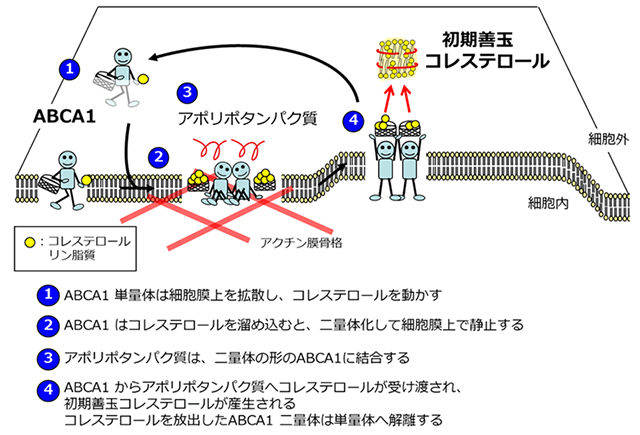
図4:ABCA1による善玉コレステロール産生モデル
さらに、蛍光標識したアポリポタンパク質を培養培地に添加すると、アポリポタンパク質が二量体の状態のABCA1に結合する様子が観察されました。一方、アポリポタンパク質はHDL産生機能をもたない変異型ABCA1には結合しませんでした。
- アポリポタンパク質は二量体の状態のABCA1に結合し、ABCA1からコレステロールを受け取る
- 溜め込んでいたコレステロールを放出したABCA1は、二量体から単量体へと解離する
では、なぜABCA1は、二量体の形となる必要があるのでしょうか? 実は、ABCA1によって産生されるHDLは、二つのアポリポタンパク質分子が合わさってコレステロールやリン脂質を束ねた構造をとっています。そこで、アポリポタンパク質分子がバラバラにABCA1からコレステロールを受け取るよりも、2分子のアポリポタンパク質が一緒になってコレステロールを受け取り、HDLを産生するほうが効率的であると考えられます。本研究チームは、ABCA1の二量体が、2分子のアポリポタンパク質を出会わせるためのプラットホームとしての意味を持っているものと考えています。HDL産生能をもたない変異型ABCA1が二量体を形成できないことからも、ABCA1の二量体化の生理学的な重要性がうかがえます。
- ABCA1の二量体化がHDL産生に重要である
今後の展開
今後はさらに、(1)ABCA1のコレステロール結合部位を同定し、ABCA1がどのようにしてコレステロールを溜め込むのか、(2)ABCA1がどのようなメカニズムによって二量体化するのか、を明らかにすることで、ABCA1によるHDL産生メカニズムをより詳細に解明することが課題となっています。
また、最近の研究によって、動脈硬化の予防のためには、HDLの量よりもHDL産生能力の方が重要だということもわかってきています。今回、本研究グループは、HDL産生の過程を可視化することに世界で初めて成功しました。今後、この過程を活性化する方法を見出すことで、動脈硬化症の予防や治療法の開発につなげることができるものと期待されます。
本研究は、文部科学省科学研究費補助金「基盤研究S」のほか、内藤記念科学振興財団および農業・食品産業技術統合研究機構生物系特定産業技術研究支援センターの支援を受けておこなわれました。
論文タイトル・著者
[DOI] http://dx.doi.org/10.1073/pnas.1220703110
"ABCA1 dimer–monomer interconversion during HDL generation revealed by single-molecule imaging"
(参考訳:HDL産生におけるABCA1二量体-単量体相互変換の1分子イメージングによる解明)
Koh O. Nagata, Chieko Nakada, Rinshi S. Kasai, Akihiro Kusumi, and Kazumitsu Ueda
Proceedings of the National Academy of Sciences of the United States of America (PNAS)
関連リンク
iCeMSウェブサイトでのニュースリリース(2013年3月12日)
http://www.icems.kyoto-u.ac.jp/j/pr/2013/03/12-nr.html
iCeMS Facebookページ
http://www.facebook.com/Kyoto.Univ.iCeMS
iCeMS Twitterアカウント
http://twitter.com/iCeMS_KU
iCeMS YouTubeチャンネル
http://www.youtube.com/user/iCeMSpr
- 京都新聞(3月12日 3面)、産経新聞(3月12日夕刊 10面)、日刊工業新聞(3月12日 25面)および科学新聞(4月5日 4面)に掲載されました。

