2012年12月5日

左から宮崎研究員、中辻拠点長、川瀬特任講師
中辻憲夫 物質-細胞統合システム拠点(iCeMS=アイセムス)拠点長・再生医科学研究所(再生研)教授、川瀬栄八郎 再生研特任講師、宮崎隆道 同研究員らは、関口清俊 大阪大学蛋白質研究所教授らと協力し、細胞接着タンパク質であるラミニンのフラグメント(断片)を用いて、これまでより安全・高効率にヒト胚性幹(ES)細胞・人工多能性幹(iPS)細胞を培養する方法を開発しました。この技術は、ヒトES/iPS細胞を創薬・細胞治療などに応用するにあたって必要とされる品質保証と大量生産に寄与することが期待されます。
本成果は、ロンドン時間12月4日16時に英科学誌「ネイチャー・コミュニケーションズ」でオンライン掲載されました。
背景と研究成果
ヒト多能性幹細胞(ES/iPS細胞など)株は、創薬や細胞治療にとって不可欠な、高品質の各種ヒト細胞を大量に生産供給できる、代替不可能な細胞リソースとして期待されています。そして、この実現化のためには多能性幹細胞の効率的な拡大培養法の確立が欠かせません。
一般的に、ヒト多能性幹細胞の培養には、適したフィーダー(支持)細胞(図1)あるいは細胞外基質が必要でしたが、従来は異種動物由来のもの(例:マトリゲル)が使われていました。また、最近は異種動物由来ではないものも見出されてきていますが、まだ十分な効果がありませんでした。したがって、大量培養の鍵となる効率的な拡大培養を行っていくためには、培養液だけではなく最適な細胞外基質の開発が急務です。
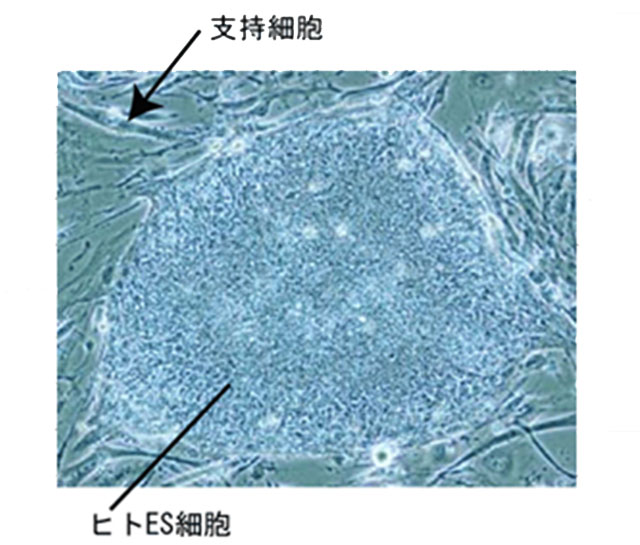
図1:ヒトES細胞、ヒトiPS細胞は写真のようにフィーダー(支持)細胞を下敷きとして増殖維持されている
また、ヒト多能性幹細胞は通常コロニー(細胞塊)として培養されています。そして継代と呼ばれる細胞を植え継ぐ過程で、このコロニーを適度な小さな塊とする必要があります。ばらばらになってしまった細胞のほとんどは死んでしまい、うまく解離できなかった大きなコロニーは分化してしまいます (図2)。このため現在行われているヒト多能性幹細胞の拡大培養法はあまり効率的ではなく、そしてその取り扱いには熟練が必要です。
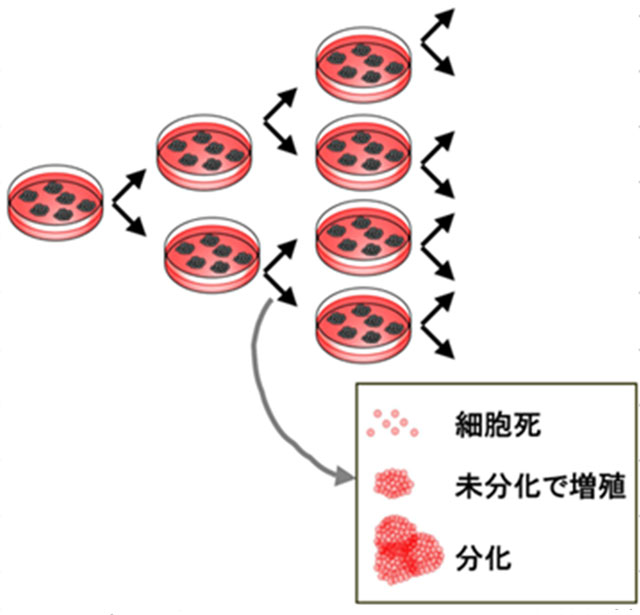
図2:ヒトES細胞、ヒトiPS細胞の拡大培養の様子
ヒト多能性幹細胞はコロニーを形成しながら増殖していくが、通常4~7日間隔で植え継いでいく必要がある。その際、細胞をばらばらに解離すると死んでしまい、また大きなコロニーのままだと分化してしまう。適度な大きさに解離することが必要だと考えられている。
本研究では、ヒト多能性幹細胞の培養の細胞外基質として現在最も使われているマトリゲルの主成分であるラミニンに着目しました。さらに、ヒトのラミニンタンパク質の中でヒト多能性幹細胞に効果のある最小の三次元部位を見出し、そのフラグメント(断片)LM-E8(図3)を調べ、ヒト多能性幹細胞に対して既存のものに比べて、細胞外基質として最も優れていることを見出しました。このLM-E8を用いることで、通常はばらばらに解離されると死んでしまうヒト多能性幹細胞でも全く問題なく接着することができ、さらに細胞同士が集まり生存し、かつ増殖していくことを見出しました(図4)。
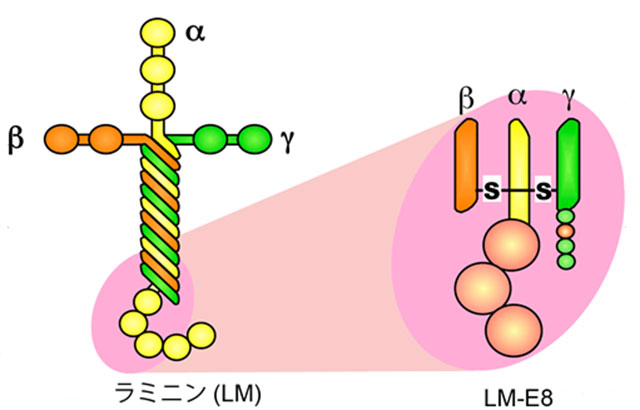
図3:左はラミニンの全体像、右は今回私達が示したヒト多能性幹細胞の
接着に必要な最小単位のフラグメント(LM-E8)
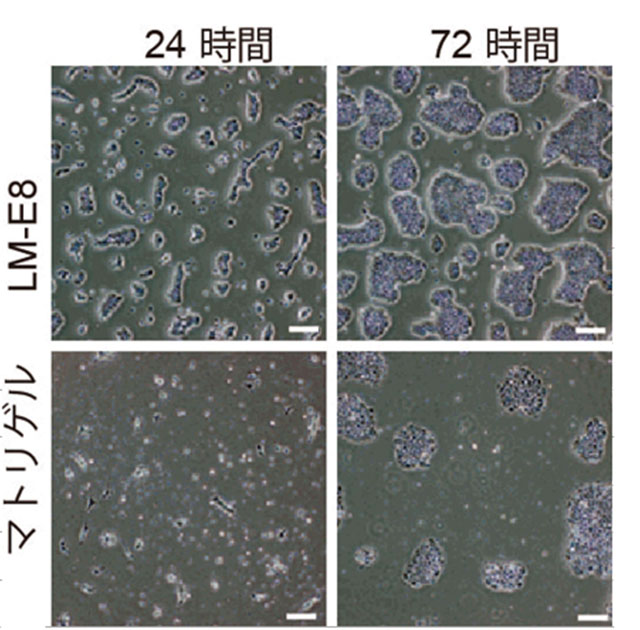
図4:従来用いられているマトリゲルに比べてLM-E8では細胞が効率良く接着、生存、増殖していく様子がわかる
このLM-E8と臨床応用にも使用可能な既知成分のみを含む培地を用い、ヒト多能性幹細胞の長期培養を行ったところ、1ヶ月間で従来法よりも200倍以上の効率で細胞増殖させることが可能になりました(図5)。そして、染色体異常などが観察されないことと、多能性幹細胞の特性も保持していることも示されました。また、本研究で使った培養法は従来に比べてはるかに簡便であり、研究者による経験の差も出にくいものです。
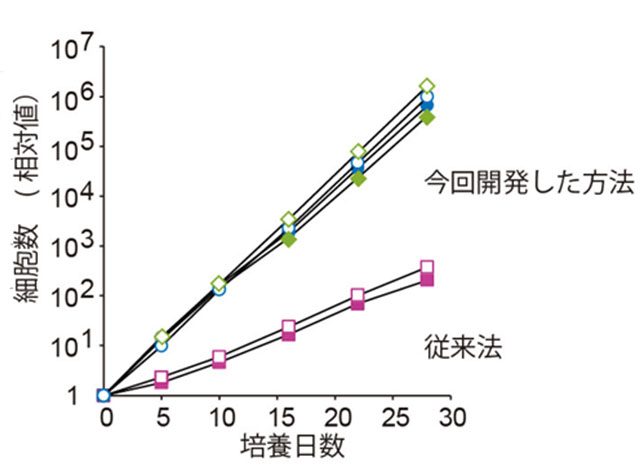
図5:従来法に比べて、1ヶ月間の培養で200倍以上の効率で細胞を拡大することができるようになった
意義と展望
本研究で確立した培養法を用いて、ヒトの多能性幹細胞を創薬スクリーニングや臨床応用に可能な品質で大量調製する技術が大きく進歩しました。今回用いたLM-E8と呼ばれるフラグメントは、ラミニン全体を調製するよりもはるかに簡単で、大量調製に適しています。また精製の過程で不純物の混入する可能性も少ない点も有利です。
再生研では、臨床応用に適した(品質保証された)ヒトES細胞株の樹立とこれを用いて臨床研究等を実施する研究機関への分配を計画しています。そのためには既知成分のみを含む培地や今回開発した培養基材などを用いて、標準化されたプロトコルによる継代培養を行うことによって、当初の樹立過程で使用された動物由来成分や特定されていない成分(リスク要因)を取り除き、将来の臨床応用に耐える品質保証されたヒトES細胞株を作成します。これと並行して、再生研ではES細胞株の樹立段階から、全て既知成分での培養を行い、アメリカの行政機関である食品医薬品局(FDA)などが要求する世界的標準条件に合致する臨床用ヒトES細胞株の樹立を計画しています。そのために、凍結余剰胚の新たな提供医療機関の選定や、インフォームドコンセントによる提供に至る手順の見直しなどを進めています。現在、日本国内ではヒトES細胞株の臨床応用にむけて「ヒト幹細胞等を用いた臨床研究に関する指針(厚生労働省)」の改訂がすすめられています。改正指針の施行後すみやかに樹立研究計画の申請を行えるよう準備を行っており、早ければ来年中の申請を見込んでいます。
注釈
マトリゲル(商品名)と呼ばれるものが最もよく使われているが、これはマウスのEHS腫瘍が分泌した細胞外基質を調製したもの。
本研究は、新エネルギー・産業技術総合開発機構(NEDO)プロジェクト「研究用モデル細胞の創製技術開発」(2005~2009年度/プロジェクトリーダー:中辻拠点長)、文部科学省「橋渡し研究支援推進プログラム」課題「多能性幹細胞フィーダーフリー培養基材の開発」(2009~2011年度/研究代表者:関口清俊)の一環として行われました。
論文タイトル・著者
[DOI] http://dx.doi.org/10.1038/ncomms2231
[KURENAIアクセスURL] http://hdl.handle.net/2433/164626
Laminin E8 fragments support efficient adhesion and expansion of dissociated human pluripotent stem cells
Takamichi Miyazaki, Sugiko Futaki, Hirofumi Suemori, Yukimasa Taniguchi, Masashi Yamada, Miwa Kawasaki, Maria Hayashi, Hideaki Kumagai, Norio Nakatsuji, Kiyotoshi Sekiguchi*, Eihachiro Kawase*
Nature Communications 3, Article number: 1236
2012/12/04/online
関連リンク
iCeMSウェブサイトでのニュースリリース(2012年12月5日)
http://www.icems.kyoto-u.ac.jp/j/pr/2012/12/05-nr.html
iCeMS Facebookページ
http://www.facebook.com/Kyoto.Univ.iCeMS
iCeMS Twitterアカウント
http://twitter.com/iCeMS_KU
iCeMS YouTubeチャンネル
http://www.youtube.com/user/iCeMSpr
- 産経新聞(12月5日 28面)、日刊工業新聞(12月5日 25面)、日本経済新聞(12月5日 42面)、毎日新聞(12月7日 4面)および読売新聞(12月5日 31面)に掲載されました。

