2012年8月2日


左から井上准教授、江川研究員
このたび、江川斉宏 iPS細胞研究所(CiRA)/科学技術振興機構(JST)CREST研究員、北岡志保 元同研究員、井上治久 CiRA/JST CREST/JST山中iPS細胞特別プロジェクト准教授の研究グループは、山中伸弥 CiRA/物質-細胞統合システム拠点/JST山中iPS細胞特別プロジェクト教授や高橋良輔 医学研究科教授らの研究グループと協力し、ALS(筋萎縮性側索硬化症)患者さんから樹立したiPS細胞を用いて、ALSのこれまで知られていなかった病態を解明し、ALSに対する新規治療薬シーズを発見しました。
この研究成果は2012年8月1日(米国東部時間)に米国科学誌「Science Translational Medicine」のオンライン版で公開されました。
要旨
ALSは運動ニューロンが変性することで次第に全身が動かなくなり死に至る疾患です。これまではALS患者さんから運動ニューロンを取り出すことができなかったために、患者さんの病態をそのまま反映するモデルを作ることが難しく、ALS治療に有効な治療薬開発は進んでいませんでした。
本研究では、TDP-43というタンパク質をコードする遺伝子に変異を持つ家族性のALS患者さんから樹立したiPS細胞を用いて、運動ニューロンを分化誘導しました(ALS運動ニューロン)。このALS運動ニューロンには、ALS病理組織の運動ニューロン内で見られるものと類似の、タンパク質の凝集体が観察されました。さらに、ALSに罹患していない運動ニューロンと比較して、突起が短く、ストレスに対して脆弱になっていました。TDP-43というタンパク質は、健常な状態ではRNAに結合して、RNAの合成・運搬等、RNA代謝に関与するとともに、TDP-43自身の発現量を自己調節していることが知られています。ALS運動ニューロンの遺伝子解析から、ALSではTDP-43の自己調節が異常をきたして、運動ニューロン内でTDP-43の発現量が増加し、神経細胞骨格の遺伝子発現や、RNA代謝に関連する分子の遺伝子発現に異常が生じていることを見いだしました。そこで、RNA代謝を調節することが知られている化合物をALS運動ニューロンに作用させたところ、それらの化合物の中でアナカルジン酸と呼ばれる化合物によって、TDP-43の発現量が低下し、ALS運動ニューロンのストレスに対する脆弱性が改善され、神経突起の長さが回復することを発見しました。
以上の結果から、ALS患者さん由来のiPS細胞から分化誘導した運動ニューロンは、ALSの治療薬シーズを探索する病態モデル系として有効であることが示され、今後の新薬開発を大きく加速することが期待されます。
本研究のポイント
- ALSは病態に未解明の部分が多いために、治療薬開発が進んでいなかった。
- ALS患者さんの細胞から樹立したヒトiPS細胞を用いて、ALS患者さんの病態を細胞レベルで再現するモデルを構築し、これまで知られていなかったALSの病態の一端を明らかにした。
- ALS患者さんのiPS細胞を用いた世界で初めてのALS治療薬シーズの発見である。
- ALSの新薬開発や発症メカニズムの解明にとって大きな一歩である。
研究の背景
ALSは50~60歳ごろから発症し、運動ニューロンが変性することで次第に全身が動かなくなる病気です。ALSの病理組織を観察すると、運動ニューロンの細胞質に凝集体が観察されます。この凝集体はTDP-43というRNA結合タンパク質が集まったものであることが明らかにされていました。これまでALS病態を示す動物モデルが報告され、その中でもALSモデルマウスを用いた研究では病状を改善する治療薬候補がいくつか同定されました。しかし、その治療薬候補の中で、ALS患者さんに投与され治療の有効性が示されたものは未だありません。そのため、動物モデルより、さらに患者さんに近いヒトの細胞系でのモデル構築が求められていました。これまでにALS患者さんからiPS細胞を樹立し、運動ニューロンへと分化誘導することは行われてきました。しかし、ALSの病態に関して不明な点が多く、どのように培養皿の中でALSの病態を再現して、治療薬候補の探索を行うべきかがわかりませんでした。
研究結果
1)ALS患者さん由来のiPS細胞を用いて病態モデルを構築
ALSに罹患していないコントロールの方5名から樹立したiPS細胞とTDP-43に変異のあるALS患者さん3名から樹立したiPS細胞を用いて、それぞれ運動ニューロンへと分化誘導させたところ、ALS患者さん由来の細胞では、コントロールの方由来の細胞と比較して、神経細胞骨格を作る遺伝子のmRNA量が低下し、神経突起が短くなっていることを明らかにしました(図1)。さらに、TDP-43のmRNA量が増加し、ALS患者さんで見られるのと同じようなTDP-43タンパク質の凝集体形成が生じていること、ストレスに対して脆弱になっていることを見いだしました。このように、ALS患者さん由来のiPS細胞を用いて、ALS病態モデルを構築することができました。
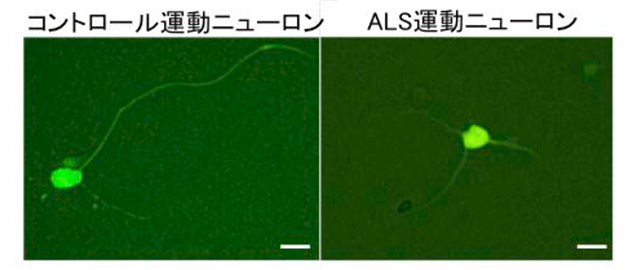
図1:運動ニューロンの突起長の比較(井上研究室提供)
2)病態モデルを用いてALSに対する新規治療薬シーズ(アナカルジン酸)を発見
遺伝子発現の解析から、ALS患者さん由来のiPS細胞から作製した運動ニューロンでは、RNAの合成や運搬(RNA代謝)に異常があると考えられました。そこで、RNA代謝に作用することが知られている四つの化合物をそれぞれ作用させたところ、アナカルジン酸には、TDP-43の発現量を低下させ、ALS運動ニューロンのストレスに対する脆弱性と神経突起の長さを改善する効果があることがわかりました。
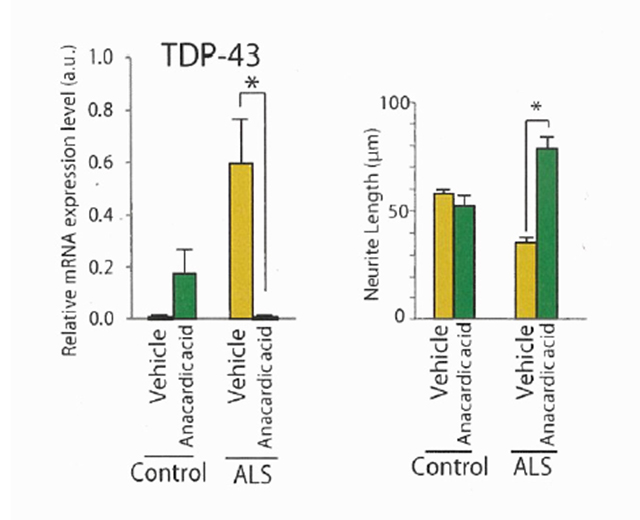
図2:アナカルジン酸の効果
左:TDP-43mRNA 量、右:神経突起の長さ
アナカルジン酸添加により、ALS運動ニューロンでTDP-43のmRNA量が減少し、神経突起の長さが伸びています。
まとめ
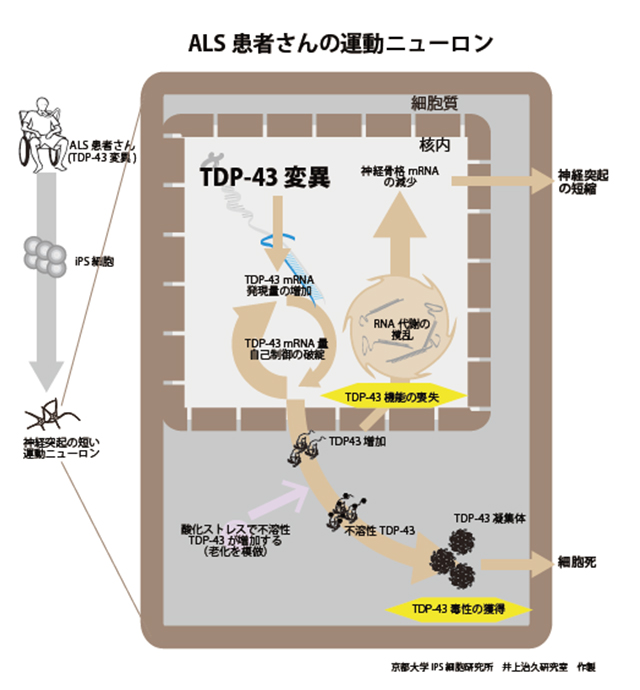
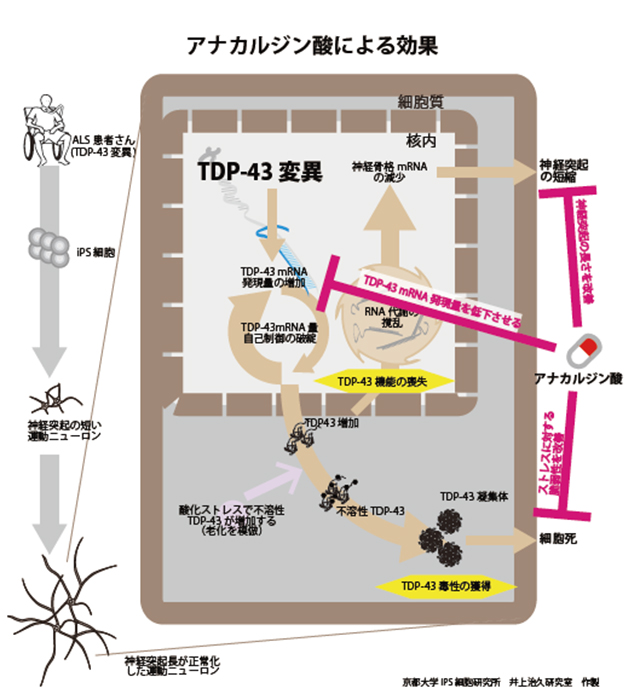
本研究では、TDP-43遺伝子変異があるALS患者さん由来のiPS細胞を用いて運動ニューロンを分化誘導し、ALSの新たな病態を明らかにしました。TDP-43タンパク質は健常な状態ではTDP-43自身の発現量を自己調節していますが、ALSではその自己調節機構に異常をきたして、運動ニューロン内でTDP-43の発現量が増加し、TDP-43が制御しているRNA合成やRNA運搬に関する遺伝子や神経細胞骨格に関する遺伝子発現の異常が生じていることがわかりました。RNA代謝に効果があるとされる化合物をALS運動ニューロンに作用させたところ、これらの異常はアナカルジン酸により抑制され、回復することを明らかにしました。
多くの孤発性のALS患者さんの病理組織の運動ニューロンにTDP-43タンパク質の凝集体がみられることから、TDP-43の異常を制御する本研究の治療薬シーズは、患者さんの大半を占める孤発性のALSにも効果があることが期待されます。今後は、患者さんのiPS細胞を用いて、病態の更なる解明を進めるとともに、治療薬シーズ探索基盤を進化させて、多くの治療薬候補を得る必要があります。
論文名と著者
[DOI] http://dx.doi.org/10.1126/scitranslmed.3004052
論文名
“Drug Screening for ALS Using Patient-Specific Induced Pluripotent Stem Cells”
ジャーナル名
Science Translational Medicine
著者
Naohiro Egawa1, 2, *, Shiho Kitaoka1, 2, *, Kayoko Tsukita1, 2, Motoko Naitoh3, Kazutoshi Takahashi1, Takuya Yamamoto1, 5, Fumihiko Adachi1, Takayuki Kondo1, 4, Keisuke Okita1, Isao Asaka1, Takashi Aoi1, Akira Watanabe1, 5, Yasuhiro Yamada1, 5, Asuka Morizane1, 6, Jun Takahashi1, 6, Takashi Ayaki4, Hidefumi Ito4, Katsuhiro Yoshikawa3, Satoko Yamawaki3, Shigehiko Suzuki3, Dai Watanabe7, Hiroyuki Hioki8, Takeshi Kaneko8, Kouki Makioka9, Koichi Okamoto9, Hiroshi Takuma10, Akira Tamaoka10, Kazuko Hasegawa11, Takashi Nonaka12, Masato Hasegawa12, Akihiro Kawata13, Minoru Yoshida14, Tatsutoshi Nakahata1, Ryosuke Takahashi4, Maria C.N.Marchetto15, Fred H.Gage15, Shinya Yamanaka1, 5, 16, Haruhisa Inoue1, 2, 16, **
*)これらの研究者はこの論文に同程度寄与しました。
**)責任著者
著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 科学技術振興機構(JST) CREST
- 京都大学大学院医学研究科形成外科
- 京都大学大学院医学研究科神経内科
- 京都大学物質ー細胞統合システム拠点(iCeMS)
- 京都大学再生医科学研究所
- 京都大学大学院医学研究科生体情報科学
京都大学大学院生命科学研究科認知情報学 - 京都大学大学院医学研究科高次脳形態学
- 群馬大学大学院医学系研究科神経内科
- 筑波大学臨床医学系神経内科
- 相模原病院神経内科
- 東京都医学総合研究所認知症・高次脳機能研究分野
- 東京都立神経病院神経内科
- 理化学研究所基幹研究所分子リガンド探索研究チーム
- ソーク研究所
- JST 山中iPS細胞特別プロジェクト
本研究への支援本研究は、下記機関より資金的支援を受けて実施されました。
- JST CREST
- JST 山中iPS細胞特別プロジェクト
- 内閣府「最先端研究開発支援プログラム(FIRST)」
- 文部科学省科学研究費補助金新学術領域研究「シナプス病態」
- 厚生労働科学研究費補助金(障害者対策総合研究事業(神経・筋疾患分野))
- ノバルティス老化および老年医学研究基金
- 朝日新聞(8月2日 33面)、 京都新聞(8月2日 1面・2面)、産経新聞(8月2日 1面)、中日新聞(8月2日 1面)、日刊工業新聞(8月2日 23面)、日本経済新聞(8月2日 1面)、毎日新聞(8月2日 2面)、読売新聞(8月2日 1面)および科学新聞(8月24日 4面)に掲載されました。

