2011年8月4日
京都大学
千葉大学
独立行政法人理化学研究所
岩田想 医学研究科教授は、村田武士 千葉大学大学院理学研究科特任准教授(独立行政法人理化学研究所生命分子システム基盤研究領域客員研究員)、水谷健二 同研究員、横山茂之 理化学研究所生命分子システム基盤研究領域長、山登一郎 東京理科大学基礎工学研究科教授との共同研究で、骨粗鬆症やがんの分子標的であるV型ATPaseの類似体と阻害剤(DCCD)の複合体構造をX線結晶構造解析により解明しました。これによりV型ATPaseを特異的に阻害するための分子機構が明らかになりました。本研究結果は、V型ATPaseの機能異常により引き起こされる上記疾病の治療薬開発に繋がるものと期待されます。
本研究は文部科学省ターゲットタンパク研究プログラム、文部科学省科学技術振興調整費(若手研究者の自立的研究環境整備促進)等の支援を受け行われました。本研究成果は、2011年8月3日(現地時間)に米国科学雑誌「米国科学アカデミー紀要(PNAS)」電子版にて公開されました。
【論文情報】
Structure of Na+-transporting vacuolar ATPase rotor ring modified with N,N' -dicyclohexylcarbodiimide. Proc. Natl Acad. Sci. USA
Kenji Mizutani, Misaki Yamamoto, Ichiro Yamato, Yoshimi Kakinuma, Mikako Shirouzu, John E. Walker, Shigeyuki Yokoyama, So Iwata, and Takeshi Murata
研究の背景と経緯
V型ATPaseは、ヒトなどの真核生物の多くの生体膜に存在し、水素イオンを運ぶことで膜内外のpHを調整しています。また、V型ATPaseは骨の形成に関わる破骨細胞やがん細胞の膜にも存在しており、骨粗鬆症やがん細胞の増殖・転移に関与していることが分かっています。そのため、V型ATPaseの分子メカニズムを知ることはこれら疾病の理解に繋がりますし、V-ATPaseの阻害剤は治療薬として期待され、製薬企業を中心に阻害剤の開発が進められています。本研究ではV型ATPaseのイオン輸送メカニズムおよび、阻害剤による阻害機構を明らかにすることを目的に、阻害剤が結合したV型ATPaseローターリング部分の立体構造の解明を試みました。
研究の内容
V型ATPaseはATPのエネルギーを使って軸と膜内ローターリングを回転させ、これにより水素イオンを膜の逆側へと輸送するポンプとして機能しています。一方、腸内連鎖球菌(Enterococcus hirae)にも哺乳類と良く似たV型ATPaseが存在し、水素イオンでなくナトリウムイオンを輸送する特徴を持っています。ナトリウムイオンは、X線結晶構造解析や放射性同位体を用いた実験において、水素イオンより検出しやすいという有利な点があります。そのため、当研究グループは腸内連鎖球菌V型ATPaseの生化学的・構造生物学的研究を進めています。そして、膜内のローターリング(Kサブユニット10個がリング状に結合したもの)が回転することによって隣接するIサブユニットとナトリウムイオンの受け渡しを行い、輸送していることが明らかになっています(図1)。
本研究ではV型ATPaseの阻害剤として知られるDCCDの阻害機構について放射性同位体(22Na+)を用いて詳細に調べました。その結果、DCCDはローターリングからナトリウムイオンが解離した状態でのみ結合することが明らかになりました。また、10ヶ所あるDCCD結合部位のうち1~2ヶ所でも結合するとV型ATPaseの活性を完全に阻害することが明らかになりました。さらに、DCCDが結合したローターリングのX線結晶構造解析に成功しました(図2)。DCCDはローターリングのナトリウム結合ポケットを塞ぐ役割をするグルタミン酸残基と共有結合していました。DCCDが結合することによってローターリングとIサブユニットとの界面で立体障害がおこり、回転が妨げられることにより機能阻害されることが立体構造から示唆されました。ナトリウムイオン存在下/非存在下で結晶化を行うことにより、ナトリウム結合型(図2C、D)および非結合型(図2E、F)のローターリングの構造を得ることができました。これにより、イオン輸送におけるグルタミン酸残基の重要性や構造変化についての理解が大きく進み、V型ATPaseの詳細なイオン輸送メカニズムを提案することができました。
今後の展開
本研究により、V型ATPaseのローターリング部分に結合する阻害剤DCCDの阻害機構が明らかになりました。他に知られているV型ATPaseの阻害剤も同様にローターリングに結合し、阻害することが予想されています。今回明らかになった知見は、V型ATPaseが関係する様々な疾病に対する薬剤の開発に役立つものと期待されます。
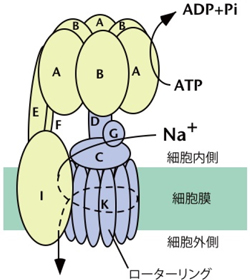
- 図1 腸内連鎖球菌V型ATPaseの構造モデル腸内連鎖球菌V型ATPaseは9種類のタンパク質(F、I、K、E、C、G、A、B、D)からなる超分子複合体で、ATPの 加水分解のエネルギーによって、中央回転軸とローターリング(青い部分)を回転させ、ナトリウムイオンを細胞外へ排出する働きを持つ。ヒトのV型ATPaseも基本的な構造は酷似している。
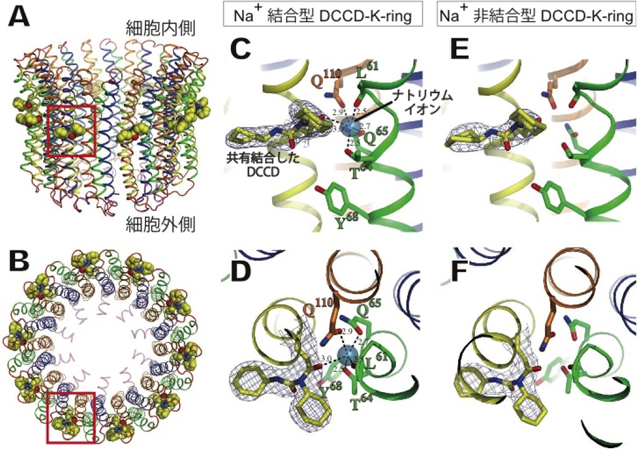
- 図2 DCCDが結合したローターリングのX線結晶構造
A) 側面から見たローターリングの構造
B) 上から見たローターリングの構造
C-F) ナトリウムイオン(Na+)存在下(C、D)および非存在下(E、F)でのDCCD結合型ローターリングのナトリウム結合ポケットの構造。
用語解説
X線結晶構造解析
解析対象のタンパク質を結晶化し、X線照射によって得られる回折データから、結晶内部で原子がどのように配列しているかを決定する手法。
放射性同位体
ラジオアイソトープとも呼ばれ、構造が不安定なため時間とともに放射性崩壊していく核種。今回使用したものは、ナトリウム22。
関連リンク
- 論文は以下に掲載されております。
http://dx.doi.org/10.1073/pnas.1103287108 - 以下は論文の書誌情報です。
Mizutani K, Yamamoto M, Suzuki K, Yamato I, Kakinuma Y, Shirouzu M, Walker JE, Yokoyama S, Iwata S, Murata T. Structure of the rotor ring modified with N,N'-dicyclohexylcarbodiimide of the Na+-transporting vacuolar ATPase. Proc Natl Acad Sci U S A. 2011 Aug 3.

