2011年2月17日
岩田想 医学研究科教授、小林拓也 同講師、島村達郎 同客員研究員、伊藤圭祐 静岡県立大学助教、伊藤創平 同助教らは、世界で初めて、虫歯の病原因子として同定されている酵素である「グルカンスクラーゼ(GSase)」の立体構造をX線結晶構造解析によって明らかとすることに成功し、この酵素による多糖の合成メカニズムを明らかにしました。
口腔中に存在する菌に由来する酵素GSaseは、砂糖から歯垢(プラーク)の基となる粘着性多糖であるグルカンを合成することから、虫歯発症の原因として知られています。これまで、GSaseの働きを阻害することが虫歯予防に効果的と考えられていましたが、GSaseと類似の酵素が口腔中や小腸等にも存在することから、GSaseの働きだけを特異的に阻害する物質でないと、類似の酵素の働きも阻害してしまい、低血糖等の弊害を引き起こす可能性があります。そこで、阻害物質のリスクを低くするために、GSaseの働きだけを特異的に阻害する物質の設計が求められており、GSaseの立体構造の解明が有効な手段として望まれていました。
本研究グループは、これまで困難であったGSaseの発現システムを構築、界面活性剤を利用した結晶化により高分解能の解析データを得ることに成功し、GSaseの立体構造を解明しました。また、GSaseの阻害剤やアクセプター基質との結合構造も解明し、分子レベルでGSaseの働きを明らかにしました。今後、虫歯の病原因子であるGSaseの立体構造情報をもとに、より選択性が高く、強くGSaseに結合する阻害物質の探索・設計が可能となり、より効果的な虫歯の予防物質の探索に役立つことが期待されます。
本研究は、阿部啓子 東京大学教授、科学技術振興機構(JST)戦略的創造研究推進事業ERATO型研究「岩田ヒト膜受容体構造プロジェクト」との共同研究として行われました。
本研究成果は、米国の科学誌「Journal of Molecular Biology」のオンライン速報版で近日中に公開されます。
(論文名)
"Crystal Structure of Glucansucrase from the Dental Caries Pathogen Streptococcus mutans"
(う蝕病原菌由来グルカンスクラーゼの結晶構造)
Ito K., Ito S., Shimamura T., Weyand S., Kawarasaki Y., Misaka T., Abe K., Kobayashi T., Cameron A.D., Iwata S. (2011) J. Mol. Biol.
研究の背景と経緯
虫歯(う蝕)は全世界人口の7割、日本人の9割が患っている最も身近な生活習慣病であり、砂糖の摂取が原因となって発症します。虫歯の進行に伴い、痛みや歯を失うだけにとどまらず、長期間の放置によって敗血症を引き起こして死亡する例も報告されています。また、虫歯発症の原因となる歯垢(プラーク)は口臭や歯周病、誤嚥性肺炎の原因ともなります。このように、虫歯の発症リスクの低減は生活の質(QOL)の向上のみならず予防医学的観点からも重要です。
これまで、虫歯の病原因子として、口腔中のストレプトコッカス・ミュータンス菌に由来する酵素であるグルカンスクラーゼ(GSase)が同定されています。口腔中に砂糖があると、まずGSaseにより粘着性多糖であるグルカンが合成されます。さらに、グルカンは食べカスや他の口腔細菌を巻き込んで歯垢を形成し、内部で口腔細菌が増殖します。 歯垢内部で口腔細菌により酸が産生されることで歯が脱灰して、虫歯が進行します(図1)。そのため、GSaseの働きを阻害することで、虫歯の発症リスクを効果的に低減することが可能です。これまで、各種食品素材等からGSase阻害物質が探索され、緑茶カテキン等のポリフェノール類に強い阻害効果があることが報告されています。しかし、より選択性が高く、強い効果を持つ阻害物質の探索・設計にはGSaseの分子基盤を明らかにする必要がありました。
本研究では、虫歯の予防(GSase阻害)物質の探索・設計への分子基盤情報を得ることを目的に、GSaseの立体構造解明を試みました。
研究の内容
今回研究グループは、ストレプトコッカス・ミュータンス菌のゲノムからGSaseをコードする遺伝子を取得し、発現領域および発現条件の最適化により、これまで困難であった均質なGSaseの大量調製に成功しました。そして、膜タンパク質の結晶化で効果をあげている界面活性剤の技術により結晶化を行い、X線結晶構造解析によってGSaseの立体構造を解明しました。また、GSaseの多糖グルカン合成メカニズムを分子レベルで解明するために、阻害剤であるアカルボース、アクセプター基質である麦芽糖との結合構造についても解析に成功しました。
GSaseの全体構造は、既知のアミラーゼに類似したTIMバレル構造を取っていましたが(図2-a)、既知アミラーゼと比較してアミノ酸配列の順列に置換が起きており(図2-b)、さらに触媒部位に被さるように二つのαヘリックスが存在していました。また、GSaseの触媒部位において、サブサイト-1の立体構造は既知アミラーゼと類似していましたが、サブサイト+1, +2, +3の構造は大きく異なっていました(図3-a)。このことは、GSaseに特異的な阻害剤の設計に重要な知見です。またGSaseのアクセプター基質である麦芽糖は、GSaseのN末端から517番目のトリプトファン残基と430番目のチロシン残基に挟まれて結合しており、これらのアミノ酸残基がアクセプター基質の結合に重要であること、さらに、アクセプター基質の結合配向には593番目のアスパラギン酸残基が重要であることも明らかとなりました(図3-b)。
今後の展開
近年、創薬分野ではタンパク質の立体構造を基にした創薬戦略(Structure-Based Drug Design)が進められています。本研究により明らかとされた虫歯の病原因子の立体構造情報を利用することで、より特異性の高く効果の強い虫歯の予防(GSase阻害)物質の探索・設計が可能になり、歯周病と並んで歯科の二大疾患であり、最も身近な生活習慣病でもある虫歯の予防への貢献が期待されます。また、緑茶カテキンに代表される既知のGSase阻害物質についても、阻害効果の科学的根拠が明らかになると期待されます。
参考図
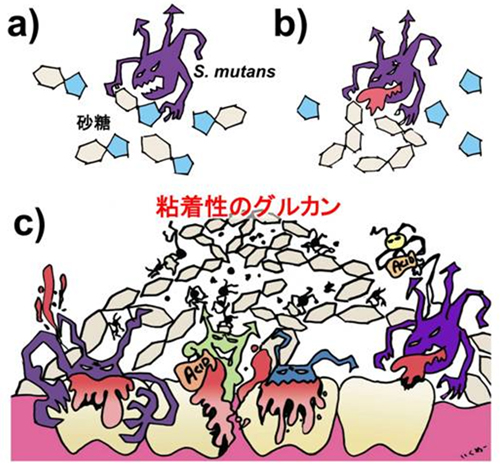
- 図1. 虫歯の発症メカニズム
a) 口腔中にストレプトコッカス・ミュータンス菌が存在する状態で砂糖を摂取する。b) ストレプトコッカス・ミュータンス菌が産生するGSaseにより砂糖から粘着性多糖であるグルカンが合成される。c) グルカンに食べカスや他の口腔細菌が巻き込まれ、歯垢が形成され、口腔細菌により酸が産生されることで歯が脱灰し、虫歯が進行する。
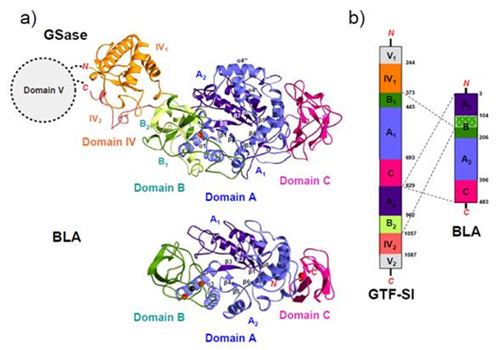
- 図2. GSaseの全体構造
a) GSaseと既知のアミラーゼ(BLA: Bacillus licheniformis α-amylase)の構造比較。Domain A, B, Cの構造は全体的に類似していたが、GSaseには既知のアミラーゼにはない2つのαヘリックス(α4'とα4'')とDomain IVが存在した。Domain Vは本研究では明らかとしていない。b) アミノ酸配列とDomain構造の比較。GSaseでは、既知のアミラーゼと比較して、アミノ酸配列の順列に置換が起きていた。
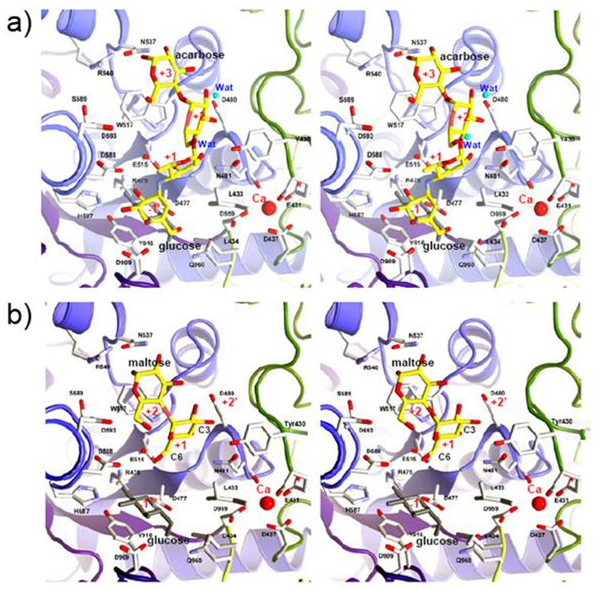
- 図3. 阻害剤、アクセプター基質との結合構造
a) GSaseの阻害剤であるアカルボースとの結合構造。サブサイト-1のアミノ酸残基は既知のアミラーゼと類似していた。一方、サブサイト+1, +2, +3のアミノ酸残基は大きく異なっていた。b) アクセプター基質である麦芽糖との結合構造。麦芽糖はN末端から517番目のトリプトファン残基と430番目のチロシン残基に挟まれて結合しており、さらに、アクセプター基質の結合配向には593番目のアスパラギン酸残基が重要であった。
用語解説
X線結晶構造解析
解析対象のタンパク質を結晶化し、X線照射によって得られる回折データから、結晶内部で原子がどのように配列しているかを決定する手法。
アクセプター基質
GSaseは砂糖をもとに、歯垢の原因となる粘着性多糖であるグルカンを合成します。その際、まずGSaseに一つめの砂糖分子(ドナー基質)が結合し、続いて次の糖(アクセプター基質:砂糖等)が結合し、ドナー基質に作用することで反応が進行します。
TIMバレル構造
αヘリックスとβストランドが交互に出現するタンパク質構造の一つ。酵素の構造において頻繁にみられる。
αヘリックス
タンパク質中にみられる二次構造で、アミノ酸の鎖(ポリペプチド)がらせん状の構造。βストランドも二次構造の一つであり、平面状の構造。
サブサイト
GSaseによる糖の加水分解部位を基点に、還元末端側の糖ユニットを認識する酵素領域を順にサブサイト+1, +2 ...、非還元末端側の糖ユニットを認識する領域を順にサブサイト-1, -2 ...と呼びます。
関連リンク
- 論文は、以下に掲載されております。
http://dx.doi.org/10.1016/j.jmb.2011.02.028
- 朝日新聞(2月18日 37面)および読売新聞(2月18日 2面)に掲載されました。

