2010年12月7日

左から本庶教授、相田特定研究員、Stanlie大学院生
本庶佑 医学研究科免疫ゲノム医学講座教授、Nasim Begum 同特定助教、相田将俊 同特定研究員(G-COE)、Andre Stanlie 同大学院生の研究グループの成果が科学誌「PNAS」の電子版で掲載されることになりました。
論文名: 「FACT複合体によって制御されるヒストンH3K4トリメチル化修飾はクラススイッチ組換えにおけるDNA鎖切断に必須である」
米国科学アカデミー紀要(Proceedings of the National Academy of Sciences of the United States of America), in press (2010)
研究の概要
クラススイッチ組換えとは、外部刺激に応じてB細胞が自身の産生する抗体分子の定常部をDNA組換えにより変化させ、その抗体が必要となる部位に適した形態(クラス)に移行させるメカニズムである。クラススイッチ組換えに伴うDNA鎖切断は抗体重鎖遺伝子座において、各クラスをコードするCセグメントの上流のスイッチ(S)領域と呼ばれる繰り返し配列周辺で起きることが分かっている。さらに、このDNA鎖切断には、i) 2000年に本庶らが発見した核酸編集酵素AIDタンパク質の発現と、ii)S領域が転写されること、の2つが必須であるこ とも良く知られている。すなわち例えば、IgMからIgG1へのクラススイッチは、外部刺激に応答して、AIDの発現とSμ領域及びSγ1領域上での転写が誘導されることで実現される(図1)。しかし、AIDによるDNA鎖切断になぜ転写が必要であるかは解明されていなかった。
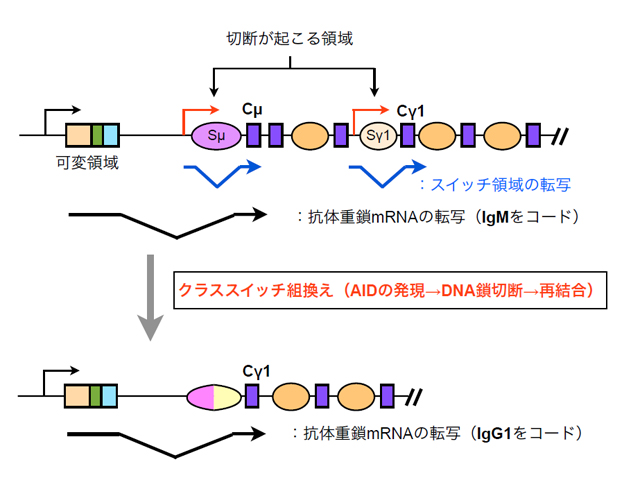
- 図1: 抗体重鎖遺伝子の構造とクラススイッチ組換えの例
今回、我々はS領域が転写される際に、FACT(facilitates chromatin transcription)複合体とよばれるタンパク質がS領域中のヌクレオソームに特定の化学修飾を発生させることでDNA鎖切断を誘導していることを明らかにし、転写とクラススイッチとの関係を解き明かした。FACT複合体はRNAポリメラーゼIIが転写を進行させる際に、DNAを巻き取っているヌクレオソーム構造を除去する機能を持つヒストンシャペロン型転写伸長因子である。FACT複合体をRNAi法によりノックダウンすると、マウスCH12細胞では、転写によるRNAの合成は阻害されずに、クラススイッチのみが阻害された。この阻害はDNA鎖切断の阻害によって引き起こされていた。次に、 S領域中のヌクレオソーム構造の変化を解析すると、ヌクレオソームの構成タンパク質であるヒストンH3の4番目のリシン残基のトリメチル化(H3K4me3)がFACTノックダウンによって極度に抑制されることが分かった。さらに、H3K4のメチル化酵素複合体を構成するAsh2LやWDR5タンパク質などをノックダウンすると、 FACTノックダウンと同様にクラススイッチが抑制された。以上により、S領域が転写される際にFACT複合体が誘導するH3K4me3修飾が、AIDが制御するDNA鎖切断のマーキングとして機能していることが示された(図2)。
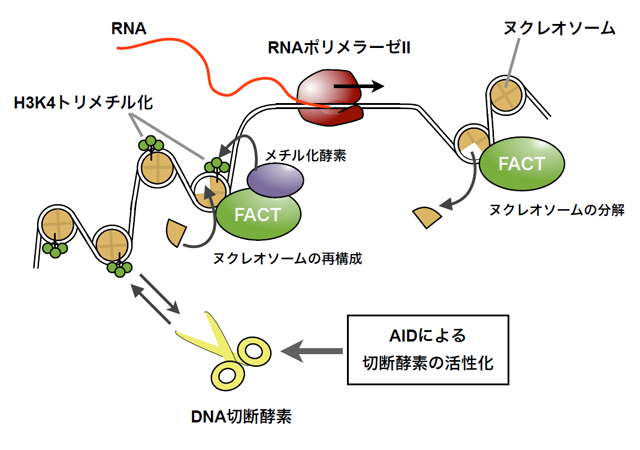
- 図2: FACT複合体によるスイッチ領域のトリメチル化がDNA切断酵素の目印になっている
H3K4のメチル化のDNA組換えにおけるマーキングとしての機能は、V(D)J組換えや減数分裂組換えなど、他のDNA組換え機構にも利用されていることが分かっている。したがって、これらの組換え機構は目的は違えど、根本的には類似した原理の上に成り立っていると考えられる。今後、H3K4me3のマーキングの認識機構などを解明することによって、今回の発見は将来的には、アレルギー疾患などクラススイッチ異常が関わると思われる疾患の治療法や、ゲノムDNAを人工的に編集する技術の確立に貢献するものと考えられる。
関連リンク
- 論文は、以下に掲載されております。
http://dx.doi.org/10.1073/pnas.1016923108 - 以下は論文の詳しい書誌情報です。
Stanlie A, Aida M, Muramatsu M, Honjo T, Begum NA. Histone3 lysine4 trimethylation regulated by the facilitates chromatin transcription complex is critical for DNA cleavage in class switch recombination [Internet]. Proceedings of the National Academy of Sciences [Published online before print December 7, 2010].
- 朝日新聞(12月14日 20面)、京都新聞(12月7日 27面)および日刊工業新聞(12月7日 22面)に掲載されました。

