浜地格 工学研究科教授、田村朋則 同助教らの研究グループは、生きた細胞内の狙った天然タンパク質を高速かつ高選択的に化学修飾することが可能な新たな手法を開発しました。さらに本手法は、標的タンパク質の活性のコントロールにも応用可能であり、それにより、ガンの創薬ターゲットである熱ショックタンパク質90(Hsp90)の不可逆阻害剤の開発に世界で初めて成功しました。
本研究成果は、2018年5月14日に国際学術誌「Nature Communications」でオンライン公開されました。
研究者からのコメント

左から、浜地教授、 田村助教
私たちの研究グループでは、以前から細胞内に存在する内在性(天然)のタンパク質を選択的に化学修飾することに成功していましたが、修飾反応があまりに遅く、使い勝手の悪さを感じていました。本研究では、従来タンパク質修飾に使えるとは考えられていなかった反応基を我々の手法に取り入れることで、修飾にかかる時間が大幅に短縮されただけではなく、修飾効率も飛躍的に向上しました。これがブレークスルーとなり、創薬ターゲットとして有望視されているHsp90の不可逆阻害に世界で初めて成功しました。
今回開発した手法は合成化学者の分子設計次第で様々なタンパク質へと展開可能であることから、不可逆阻害剤開発のための一般性の高い戦略として創薬研究を加速することが期待されます。
概要
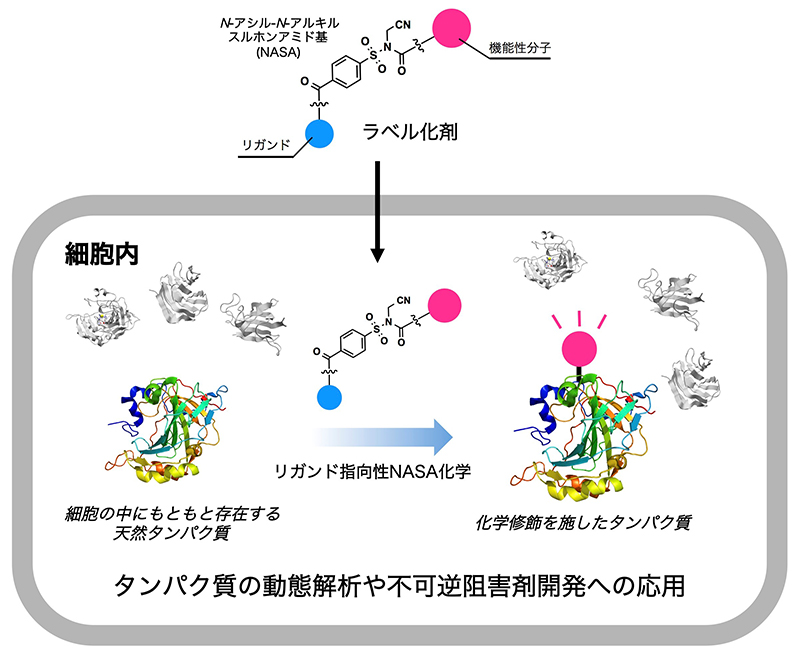
緑色蛍光タンパク質の応用でも明らかになったように、タンパク質を色々な分子で修飾することは、生命現象を解明するための強力な方法となります。しかし、ゲノム編集技術の発達した遺伝子工学とは対照的に、種々雑多な生体分子が高濃度に存在する細胞内で、狙ったタンパク質だけを選択的に修飾することは現在の化学技術をもってしても極めて困難です。本研究グループは、「リガンド指向性化学」と呼ばれる独自の戦略を開発し、細胞内タンパク質の選択的な化学修飾を実現してきました。しかしこれまでのリガンド指向性化学は修飾反応に数時間から数日の時間を要するため使い勝手が悪く、応用が限定されてしまうという大きな問題がありました。
そこで、本研究グループは新たに、酵素反応に匹敵するくらい高速の化学修飾が可能な「リガンド指向性N-アシル-N-アルキルスルホンアミド(NASA)化学」を開発しました。さらに本手法により、世界初となるHsp90不可逆阻害剤を開発しました。NASA化学は分子設計次第で他の様々な種類のタンパク質へと適用可能であり、今後、不可逆阻害剤開発のための一般性の高い戦略として創薬研究を加速することが期待されます。
詳しい研究内容について
書誌情報
【DOI】 https://doi.org/10.1038/s41467-018-04343-0
【KURENAIアクセスURL】 http://hdl.handle.net/2433/231114
Tomonori Tamura, Tsuyoshi Ueda, Taiki Goto, Taku Tsukidate, Yonatan Shapira, Yuki Nishikawa, Alma Fujisawa, Itaru Hamachi (2018). Rapid labelling and covalent inhibition of intracellular native proteins using ligand-directed N-acyl-N-alkyl sulfonamide. Nature Communications, 9, 1870.
- 日刊工業新聞(5月15日 25面)に掲載されました。