今村恵子 iPS細胞研究所(CiRA=サイラ)特定拠点助教、井上治久 同教授らの研究グループは、国内外の研究グループらとともに、ALS(筋萎縮性側索硬化症)患者さん由来iPS細胞を用いて治療薬探索のための薬剤スクリーニングを行い、ALSの治療標的となる分子経路とALS運動ニューロンの細胞死を抑える既存薬を同定しました。
本研究成果は、2017年5月25日午前3時に米国の科学誌「Science Translational Medicine」でオンライン公開されました。
研究者からのコメント

左から、井上教授、今村特定拠点助教
本研究では、 Src/c-Abl 経路が ALS の治療標的分子経路の一つである可能性を示し、 Src/c-Abl 阻害薬であるボスチニブが、 ALS 患者さんから作製した iPS 細胞由来運動ニューロンの生存率および ALS モデルマウスの生存期間を延長することを示しました。
今後はさらに病態に関連する治療標的分子について、詳細に解析したいと考えています。
本研究成果のポイント
- 筋萎縮性側索硬化症(ALS)は、運動ニューロンが変性して筋萎縮と筋力低下を来す疾患で、そのメカニズムは詳しく知られておらず、十分な治療法がない。
- SOD1遺伝子に変異を有する家族性ALS患者さん由来iPS細胞から作製した運動ニューロンを用いて、化合物スクリーニングを行い、ALS運動ニューロンの細胞死を抑える既存薬と、ALSの病態に関与する分子経路を同定した。
- 同定した既存薬は、オートファジー(細胞自身が、細胞内のタンパク質を分解するしくみの一つ)を促進することにより、異常タンパク質蓄積と細胞死を抑制した。
- 同定した既存薬は、SOD1変異を有するALSマウスや、他の変異を有する家族性ALS患者さんあるいは孤発性ALS患者さん由来運動ニューロンでも有効性を認めた。
概要
ALSは、運動ニューロンが進行性に変性して筋萎縮と筋力低下を来す疾患で、そのメカニズムは詳しく知られておらず、まだ十分な治療法がありません。ALSはほとんどの場合が孤発性ですが、家族性では、遺伝要因としてSOD1遺伝子やTDP-43遺伝子の傷(変異)、C9orf72遺伝子内のくり返し配列の伸長などが知られています。
本研究グループは、SOD1遺伝子に変異を有する家族性ALS患者さんから作製したiPS細胞、遺伝子変異を修復したiPS細胞と健康な方から作製したiPS細胞(対照群)に、Lhx3、Ngn2、Isl1という三つの転写因子(DNAからメッセンジャーRNAへの転写開始に関わるタンパク質因子)を加えて運動ニューロンへと変化(分化)させました。すると、患者さん由来運動ニューロンでは異常に折りたたまれたタンパク質が蓄積し、細胞死を起こしやすいことが分かりました。そこで、ALS患者さんの運動ニューロンの細胞死を抑制する化合物を見つけるため、SOD1変異を有する家族性ALS患者さん由来運動ニューロンを用いて、細胞死を標的としたスクリーニング系を構築しました。既存薬を含む1,416個の化合物について、運動ニューロンの細胞死を抑えるかどうかのスクリーニングを行ったところ、27個の薬が細胞死を強く抑えました。また、その約半数がSrc/c-Ablというタンパク質の分子経路に関連していることが分かりました。
さらに、細胞死を強く抑える化合物の中で、慢性骨髄性白血病の治療薬として用いられているボスチニブという既存薬は、オートファジーといわれる不要なタンパク質を分解する働きを促進し、ALSの病態の一つである異常に折りたたまれたタンパク質を減らすことが分かりました。ボスチニブを、SOD1変異を有するALSマウスに投与したところ、有効性を示しました。さらに、TDP-43遺伝子変異あるいはC9orf72リピート伸長を有する家族性ALS患者さん由来iPS細胞から作製した運動ニューロンや、孤発性ALS患者さん由来iPS細胞から作製した運動ニューロンの一部でもボスチニブが細胞死を抑制することが分かりました。本研究は、今後のALSの治療薬開発研究に貢献するものと期待されます。
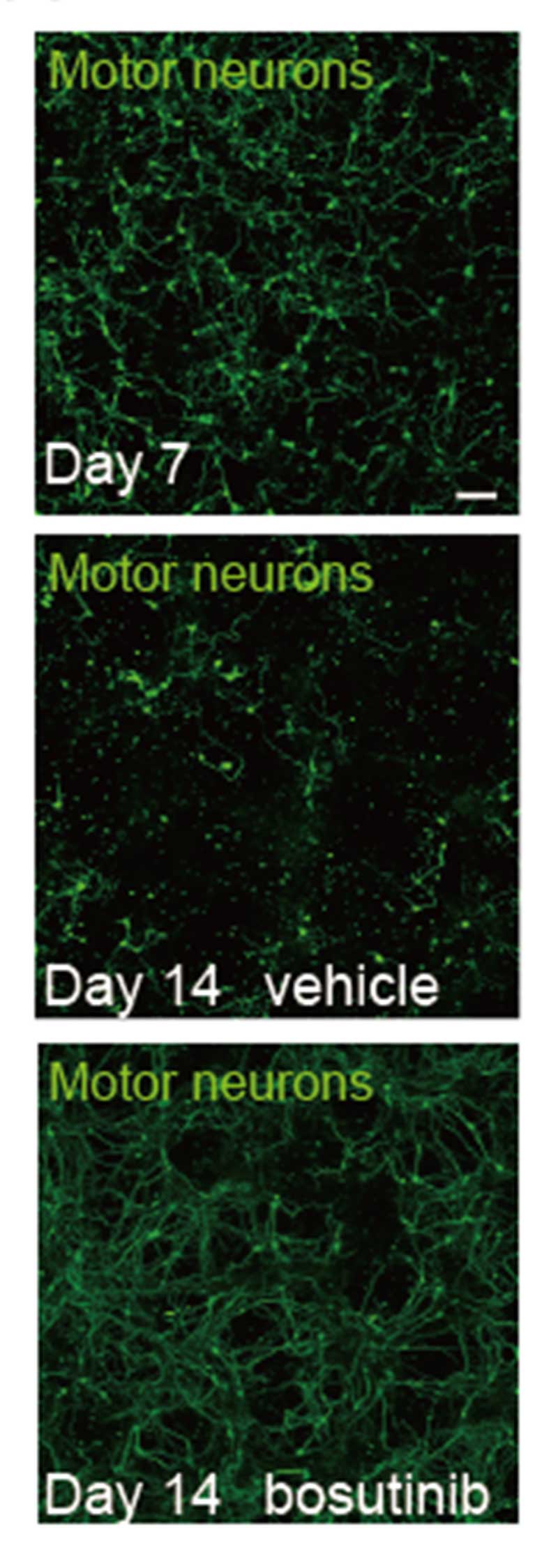
図:ALS運動ニューロンの染色像(スケールバー;100μm)
(上)iPS細胞から分化7日目のALS運動ニューロン
(中)化合物を投与しない場合のALS運動ニューロン(14日目)
(下)ボスチニブを投与した場合のALS運動ニューロン(14日目)
詳しい研究内容について
書誌情報
【DOI】 https://doi.org/10.1126/scitranslmed.aaf3962
Keiko Imamura, Yuishin Izumi, Akira Watanabe, Kayoko Tsukita, Knut Woltjen, Takuya Yamamoto, Akitsu Hotta, Takayuki Kondo, Shiho Kitaoka, Akira Ohta, Akito Tanaka, Dai Watanabe, Mitsuya Morita, Hiroshi Takuma, Akira Tamaoka, Tilo Kunath, Selina Wray, Hirokazu Furuya, Takumi Era, Kouki Makioka, Koichi Okamoto, Takao Fujisawa, Hideki Nishitoh, Kengo Homma, Hidenori Ichijo, Jean-Pierre Julien, Nanako Obata, Masato Hosokawa, Haruhiko Akiyama, Satoshi Kaneko, Takashi Ayaki, Hidefumi Ito, Ryuji Kaji, Ryosuke Takahashi, Shinya Yamanaka and Haruhisa Inoue (2017). The Src/c-Abl pathway is a potential therapeutic target in amyotrophic lateral sclerosis. Science Translational Medicine, 9(391), eaaf3962.
- 朝日新聞(5月25日夕刊 11面)、京都新聞(5月25日 25面)、産経新聞(5月25日 1面、27面)、日刊工業新聞(5月25日 23面)、日本経済新聞(5月25日 38面)、毎日新聞(5月25日 28面)および読売新聞(5月25日 31面)に掲載されました。