日野恭介 iPS細胞研究所共同研究員(大日本住友製薬株式会社先端創薬研究所)、池谷真 同准教授、戸口田淳也 同教授らの研究グループは、FOP患者さんから作製したiPS細胞(FOP-iPS細胞)を分化させて作製したFOP患者さん由来細胞(FOP細胞)を用いて、本来別のシグナルを伝える分子であるアクチビンAが、FOP細胞ではBMPシグナルを異常に伝達し、骨軟骨形成を促進することを示しました。
本研究成果は2015年11月30日(米国東部時間)に「Proceedings of the National Academy of Sciences(米国科学アカデミー紀要)」で公開されました。
研究者からのコメント

左から日野研究員、池谷准教授、戸口田教授
本研究では、FOP-iPS細胞を用いて、本来TGF-βシグナルを伝える分子であるアクチビンAがFOP細胞ではBMPシグナルを伝え、骨軟骨形成を促進することを明らかにし、このメカニズムがFOPにおける異所性骨化形成に大きく寄与している可能性を示しました。またこの結果は、アクチビンA阻害剤がFOP治療薬の候補となる可能性を示唆します。
本研究成果のポイント
- 進行性骨化性線維異形成症(Fibrodysplasia Ossificans Progressiva; FOP)患者さんから作製したiPS細胞を用いることにより、通常では他のシグナルを伝達するアクチビンAが、疾患細胞ではBMPシグナルを異常に伝達し、異所性骨形成を促進することを明らかにした。
- アクチビンA阻害剤がFOP治療薬となる可能性が示された。
- 疾患iPS細胞から作製した間葉系間質細胞を、アクチビンA発現細胞と共に免疫不全マウスに移植し、患者さん由来細胞を用いた異所性骨形成モデルの作製に世界で初めて成功した。
概要
FOPとは、筋肉や腱、靭帯など本来は骨が出来てはいけない組織の中に異所性骨とよばれる骨が徐々にできる疾患です。原因は、BMP受容体であるACVR1の一部が突然変異により変化して、BMPシグナルを過剰に伝えるためと考えられていますが、発症に至る詳しいメカニズムは分かっていませんでした。
このたび、本研究グループはFOP-iPS細胞を用いて、本来は別のシグナルを伝えるアクチビンAが、FOP細胞ではBMPシグナルを異常に伝達することを突き止めました。さらにFOP-iPS細胞から作製した間葉系間質細胞を、アクチビンA発現細胞とともに免疫不全マウスに移植することで、患者由来細胞を用いた異所性骨形成モデルの作製に世界で初めて成功しました。これらの結果はアクチビンAの阻害剤がFOP治療薬の候補となる可能性を示唆しており、異所性骨形成モデルを用いて治療候補薬の効果を生体で検証することが可能となりました。
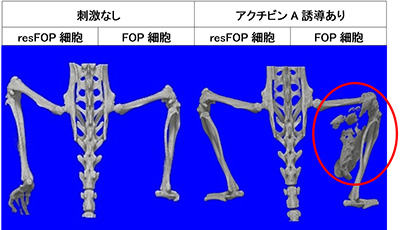
FOP-iPS細胞由来間葉系間質細胞を用いた異所性骨モデル
FOP細胞を移植しアクチビンAを誘導した場合のみ、異所性骨が形成されました。
詳しい研究内容について
書誌情報
[DOI] http://dx.doi.org/10.1073/pnas.1510540112
Kyosuke Hino, Makoto Ikeya, Kazuhiko Horigome, Yoshihisa Matsumoto, Hayao Ebise, Megumi Nishio, Kazuya Sekiguchi, Mitsuaki Shibata, Sanae Nagata, Shuichi Matsuda, and Junya Toguchida
"Neofunction of ACVR1 in fibrodysplasia ossificans progressiva"
PNAS, published ahead of print November 30, 2015
- 朝日新聞(12月1日 33面)、京都新聞(12月1日 27面)、産経新聞(12月1日 24面)、日刊工業新聞(12月1日 31面)、毎日新聞(12月1日 6面)および読売新聞(12月1日 33面)に掲載されました。