2010年11月24日
増谷弘 ウイルス研究所准教授、吉原栄治 生命科学研究科博士後期課程大学院生らのグループが藤本新平 医学研究科糖尿病・栄養内科学准教授、稲垣暢也 同教授らとの共同研究で行った研究成果が、科学誌「Nature Communications」電子版に11月23日(日本時間11月24日)に掲載されました。
タイトル: Thioredoxin binding protein-2 (TBP-2)の阻害は肥満であってもインスリンの感受性と分泌を増強させることによって2型糖尿病を改善する
英文タイトル:Disruption of TBP-2 ameliorates insulin sensitivity and secretion without affecting obesity
著者: Eiji Yoshihara, Shimpei Fujimoto, Nobuya Inagaki, Katsuya Okawa, So Masaki, Junji Yodoi & Hiroshi Masutani
研究成果の概要
生体内のグルコースホメオスタシスは、膵β細胞からのインスリン分泌量と末梢組織(骨格筋、肝臓、脂肪組織等)でのグルコース取り込み、消費量(インスリン感受性)によって厳密に制御されている。一方、過栄養状態になり脂肪が肥大化すると、脂肪細胞から分泌されるアディポサイトカインの影響を受け、膵β細胞からのインスリンの分泌と末梢組織でのインスリン感受性がともに悪化し高血糖を特徴とする2型糖尿病を引き起こすことが知られている。
本研究は、藤本准教授、稲垣教授らとの共同研究で、2型糖尿病モデル(ob/ob)マウスにおけるthioredoxin binding protein-2 (TBP-2)/thioredoxin interacting protein (Txnip) の欠損は、肥満であっても糖尿病を発症しないということを明らかにした。ob/obマウスの膵β細胞を含む膵島や骨格筋において、TBP-2の発現が顕著に亢進していた。TBP-2を欠損させたマウスは骨格筋でのIRS-1/Akt signalingの活性化を伴ってインスリンの感受性が亢進しており、膵β細胞においてはミトコンドリア脱共役因子uncoupling protein-2(UCP-2)の発現抑制を伴って、グルコース刺激性のインスリン分泌が改善することが明らかとなった。また膵β細胞株においてドキシサイクリン除去によりTBP-2発現を亢進させると、グルコースによるATP産生、Ca2+流入やインスリン分泌を抑制することが明らかとなった。TBP-2の発現誘導はUCP-2のタンパク質量、mRNA量をともに増加させ、peroxisome proliferator-γ co-activator-1α (PGC-1α)のUCP-2プロモーター上へのリクルートの増加が起こっていることが明らかとなった。さらにTBP-2は膵β細胞株においてPGC-1αの結合タンパク質であり、PGC-1αの機能阻害分子であるMybbp1aと結合していることが明らかになり、またMybbp1aはPGC-1αのUCP-2転写活性化能を阻害するが、TBP-2との共発現ではその機能を失うことが示された。これらの結果はTBP-2/PGC-1α/Mybbp1a/UCP-2を介した新たなインスリン分泌制御機構の存在を示している。これらの結果よりTBP-2はインスリンの分泌反応と感受性の両方の制御に関与し、糖尿病病態の発症もしくは悪化に関与している分子であることが示唆された。
本研究はTBP-2を標的とした新たな糖尿病治療薬開発の可能性を示唆している。
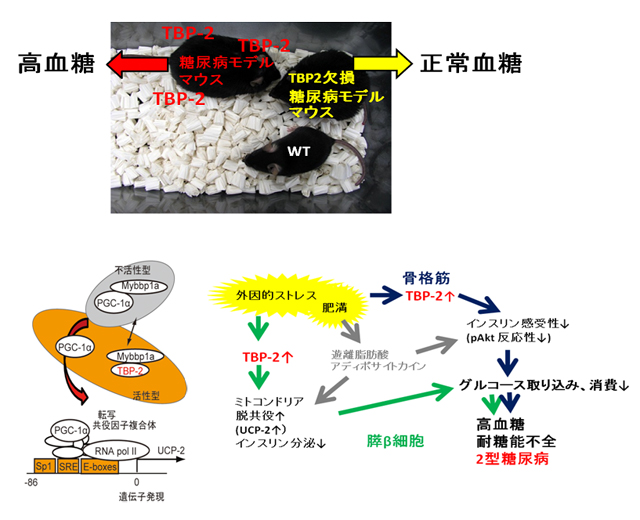
- 図 TBP-2/Txnipによるグルコースメタボリズムの制御と糖尿病発症機構
関連リンク
- 論文は以下に掲載されております。
http://www.nature.com/ncomms/journal/v1/n8/full/ncomms1127.html
- 朝日新聞(11月26日夕刊 9面)、京都新聞(11月26日 25面)、産経新聞(11月26日 25面)、日刊工業新聞(11月26日 22面)、日本経済新聞(11月26日夕刊 22面)、毎日新聞(11月26日 2面)および科学新聞(12月17日 4面)に掲載されました。

